
分析 先计算出120g碳完全燃烧放出的热量,然后根据“100gCaCO3(s)分解生成CaO(s)和CO2(g)需要吸收178kJ热量”计算出碳酸钙分解的质量.
解答 解:120gC完全燃烧放出的热量为:393.5kJ×$\frac{120g}{12g}$=3935kJ,
100gCaCO3(s)分解生成CaO(s)和CO2(g)需要吸收178kJ热量,则120gC完全燃烧放出热量能够分解碳酸钙的物质的量为:100g×$\frac{3935kJ}{178kJ}$=2.2×103g,
答:120gC完全燃烧放出的热量可使2.2×103g CaCO3分解.
点评 本题考查反应热的计算,题目难度不大,明确碳酸钙分解需要的热量等于碳燃烧放出的热量为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力.


科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液中加入稀 HCl:CO23-+2H+═H2O+CO2↑ | |
| B. | 将 NaHSO4与 Ba(OH)2溶液混合至中性:2H++SO24-+Ba2++2OH-═BaSO4↓+2H2O | |
| C. | 苯酚钠溶液中通入少量 CO2气体:2C6H5O-+CO2+H2O→2C6H5OH+CO23- | |
| D. | 用惰性电极电解氯化铝溶液:2Cl-+2H2O═Cl2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
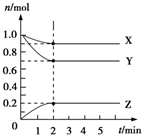 Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
Ⅰ.控制变量法是化学实验的一种常用方法.如表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 | m1 |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 | m2 |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | m3 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | m5 |
| 6 | 50.0 | 8.0 | 粉末 | 25 | t6 | 16.1 |
| 7 | 50.0 | 10.0 | 粉末 | 25 | t7 | 16.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
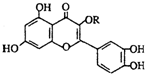 唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )
唐山市的市树是国槐,天然维生素P(结构如图)存在于国槐树花蕾中,它是一种营养增补剂.关于维生素P的叙述正确的是( )| A. | 若R为甲基则该物质的分子式可以表示为C16H10O7 | |
| B. | 分子中有三个苯环 | |
| C. | lmol该化合物与NaOH溶液作用消耗NaOH的物质的量以及与氢气加成所需的氢气的物质的量分别是4 mol、8 mol | |
| D. | lmol该化合物最多可与2molBr2完全反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KCl固体 | B. | K2SO4溶液 | C. | 铁粉 | D. | KNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH2CH3 | B. | CH3CH(CH3)CH3 | C. | C(CH3)4 | D. | CH3CH(CH3)CH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com