
| ³É·Ö | CaO | SiO2 | Al2O3 | Fe2O3 | MgO | CaS | ĘäĖū²»ČÜÓŚĖįµÄĪļÖŹ |
| ÖŹĮæ·ÖŹż£Ø%£© | 65”«66 | 3.5”«5.0 | 1.5”«3.5 | 0.2”«0.8 | 0.2”«1.1 | 1.0”«1.8 | 23-26 |

·ÖĪö ·ÖĪöĮ÷³ĢµēŹÆ½¬¼ÓČėĖįŃõ»ÆøĘ£¬Ńõ»ÆĀĮŃõ»ÆĢśŃõ»ÆĆ¾Įņ»ÆøĘČÜÓŚĖį³Į½µŗó¹żĀĖµĆµ½ĀĖŌüĪŖ¶žŃõ»Æ¹čŗĶ²»ČÜŠŌŌÓÖŹ£¬¼ÓČė»īŠŌĢæĶŃÉ«¹żĀĖŗóŌŁAÖŠÕō·¢ÅØĖõµĆµ½¾§Ģ壬BÖŠ¹żĀĖµĆµ½¾§Ģ壬ĶعżCĶŃĖ®øÉŌļµĆµ½²śĘ·£»
£Ø1£©ŅņŅŖÉś²śCaCl2£¬ĖłŅŌӦєÓĆŃĪĖį£»
£Ø2£©»īŠŌĢæ¾ßÓŠĪüø½ŠŌ£®“ÓAŗóæ“£¬ŹĒ½į¾§³Ų£¬¹ŹAÓ¦ĪŖÕō·¢ÅØĖõ£®“ÓBÖŠÓŠÄøŅŗ³öĄ“£¬¹ŹBĪŖ¹żĀĖĘ÷£®BÖŠµĆµ½¾§Ģ壬ĖłŅŌŠčŅŖĶŃĖ®øÉŌļ£¬²ÅÄܵƵ½CaCl2²śĘ·£»
£Ø3£©H2SĪŖĖįŠŌĘųĢ壬ӦÓĆ¼īŅŗĪüŹÕ£»
£Ø4£©Éč±øBÖŠ²śÉśµÄÄøŅŗŗ¬ÓŠĀČ»ÆĪļ£¬»ŲŹÕĄūÓĆ£¬æÉŅŌ½µµĶ·ĻĘśĪļÅÅ·ÅĮ棬Ģįøß¾¼ĆŠ§Ņę£»
£Ø5£©ĀČ¼ī¹¤ŅµÖŠµē½ā±„ŗĶŹ³ŃĪĖ®£¬Ńō¼«ŹĒĀČĄė×ÓŹ§µē×ÓÉś³ÉĀČĘų£¬Ņõ¼«ŹĒĒāĄė×ӵƵ½µē×ÓÉś³ÉĒāĘų£®
½ā“š ½ā£ŗ£Ø1£©ŅņŅŖÉś²śCaCl2£¬¹ż³ĢÖŠ²»ŅżČėŠĀµÄŌÓÖŹĄė×Ó£¬ĖłŅŌӦєÓĆŃĪĖį£¬¹Ź“š°øĪŖ£ŗŃĪĖį£»
£Ø2£©»īŠŌĢæ¾ßÓŠĪüø½ŠŌ£¬æÉŅŌ½ųŠŠČÜŅŗĶŃĖ®£®AŗóŹĒ½į¾§³Ų£¬¹ŹAÓ¦ĪŖÕō·¢ÅØĖõ£»“ÓBÖŠÓŠÄøŅŗ³öĄ“£¬¹ŹBĪŖ¹żĀĖĘ÷£®BÖŠµĆµ½¾§Ģ壬ĖłŅŌŠčŅŖĶŃĖ®øÉŌļ£¬²ÅÄܵƵ½CaCl2²śĘ·£¬
¹Ź“š°øĪŖ£ŗ»īŠŌĢ棻Õō·¢ÅØĖõ£»¹żĀĖĘ÷£»ĶŃĖ®øÉŌļ£»
£Ø3£©H2SĪŖĖįŠŌĘųĢ壬ӦÓĆ¼īŅŗĪüŹÕ£¬¹ŹŃ”ŹÆ»ŅČ飬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖCa£ØOH£©2+H2S=CaS+2H2O£¬
¹Ź“š°øĪŖ£ŗC£»Ca£ØOH£©2+H2S=CaS+2H2O£»
£Ø4£©Éč±øBÖŠ²śÉśµÄÄøŅŗŗ¬ÓŠĀČ»ÆĪļ£¬»ŲŹÕĄūÓĆ£¬æÉŅŌ½µµĶ·ĻĘśĪļÅÅ·ÅĮ棬Ģįøß¾¼ĆŠ§Ņę£¬
¹Ź“š°øĪŖ£ŗ¶ŌÄøŅŗ»ŲŹÕĄūÓĆ£¬½µµĶ·ĻĘśĪļÅÅ·ÅĮ棬Ģįøß¾¼ĆŠ§Ņę£»
£Ø5£©ĀČ¼ī¹¤ŅµÖŠµē½ā±„ŗĶŹ³ŃĪĖ®£¬Ńō¼«ŹĒĀČĄė×ÓŹ§µē×ÓÉś³ÉĀČĘų£¬µē½ā·“Ó¦ĪŖ£ŗ2Cl--2e-=Cl2”ü£¬Ņõ¼«ŹĒĒāĄė×ӵƵ½µē×ÓÉś³ÉĒāĘų£¬µē½ā·“Ó¦ĪŖ£ŗ2H++2e-=H2”ü£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗ2Cl-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$2OH-+H2”ü+Cl2”ü£¬
¹Ź“š°øĪŖ£ŗ2Cl-+2H2O$\frac{\underline{\;Ķصē\;}}{\;}$2OH-+H2”ü+Cl2”ü£®
µćĘĄ ±¾ĢāŅŌ”°ÓƵēŹÆ½¬æÉÉś²śĪŽĖ®CaCl2”±ĪŖŌŲĢå£¬æ¼²éŹµŃ黳±¾²Ł×÷ŗĶ¼¼ÄÜ£¬Éę¼°¹¤ŅÕĮ÷³ĢµÄĄķ½ā”¢ĪļÖŹ·ÖĄėĢį“攢ŌŖĖŲ»ÆŗĻĪļŠŌÖŹµČ£¬ŹŌĢāÄѶČÖŠµČ£¬ŹĒ¶Ōѧɜ×ŪŗĻÄÜĮ¦µÄ漲飬ŠčŅŖѧɜ»ł±¾ÖŖŹ¶µÄ»ł“”Óė·ÖĪöĪŹĢā”¢½ā¾öĪŹĢāµÄÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ŅŅ±½“ß»ÆĶŃĒāÖʱ½ŅŅĻ©·“Ó¦£ŗ
ŅŅ±½“ß»ÆĶŃĒāÖʱ½ŅŅĻ©·“Ó¦£ŗ CH2CH3£Øg£©$\stackrel{“߻ƼĮ}{?}$
CH2CH3£Øg£©$\stackrel{“߻ƼĮ}{?}$ CH=CH2£Øg£©+H2£Øg£©
CH=CH2£Øg£©+H2£Øg£©| »Æѧ¼ü | C-H | C-C | C=C | H-H |
| ¼üÄÜ/kJ•mol”„1 | 412 | 348 | 612 | 436 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ņ½ÓĆ¾Ę¾«ŹĒÓƵķ·ŪĄąÖ²Īļ·¢½Ķ¾ÕōĮóÖĘ³É£¬ÅضČĶس£ŹĒ75% | |
| B£® | ÓĆ½žÅŻ¹żøßĆĢĖį¼ŲČÜŅŗµÄ¹čŌåĶĮ±£ĻŹĖ®¹ū£¬Ęä×÷ÓĆŹĒĪüŹÕ²¢Ńõ»ÆĖ®¹ūŹĶ·Å³öµÄŅŅĻ© | |
| C£® | ”°ŗ£Ė®µ»Æ”±æÉŅŌ½ā¾ö”°µĖ®¹©Ó¦Ī£»ś”±£¬Ļņŗ£Ė®ÖŠ¼ÓČėĆ÷·ÆæÉŅŌŹ¹ŗ£Ė®µ»Æ | |
| D£® | ŹÆÓĶĮŃ½ā”¢ĆŗµÄøÉĮó”¢ÓńĆ×ÖĘ“¼”¢µ°°×ÖŹµÄ±äŠŌ¶¼ŹĒ»Æѧ±ä»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
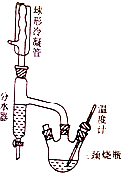 ŹµŃéŹŅÖʱøÕż¶”ĆѵÄŌĄķČēĻĀ£ŗ
ŹµŃéŹŅÖʱøÕż¶”ĆѵÄŌĄķČēĻĀ£ŗ| ĪļÖŹ | ĆܶČ/g•mL-1 | ČŪµć/”ę | ·Šµć/”ę | Ė®ČÜŠŌ |
| Õż¶”“¼ | 0.81 | -89.8 | 117.7 | Ī¢ČÜÓŚĖ® |
| Õż¶”ĆŃ | 0.769 | -98 | 142 | ²»ČÜÓŚĖ® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ū¢Ż | B£® | ¢Ś¢Ü¢Ż | C£® | ¢Ś¢Ū¢Ü | D£® | ¢Ś¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 »ÆŗĻĪļAX3ŗĶµ„ÖŹX2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦æÉÉś³É»ÆŗĻĪļAX5£®»Ų“šĻĀĮŠĪŹĢā£ŗ
»ÆŗĻĪļAX3ŗĶµ„ÖŹX2ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦æÉÉś³É»ÆŗĻĪļAX5£®»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com