
����Ŀ��(��)ijѧ����0.200 0 mol��L��1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ�����Ϊ���¼�����
��������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶�������
�ڹ̶��õζ��ܲ�ʹ�ζ��ܼ������Һ��
�۵���Һ������0������0���̶������£������¶���
����ȡ20 .00 mL����Һע��ྻ����ƿ�У�������3�η�̪��Һ
���ñ�Һ�ζ����յ㣬���µζ���Һ�����
��ش�
��1�����ϲ����д������(����)________���ô�������ᵼ�²ⶨ���(����ƫ��������ƫС��������Ӱ����)________��
��2��������У��ڼ��µζ���Һ�����ʱ���ζ��ܼ��������ݣ��ⶨ���(����ƫ��������ƫС��������Ӱ����)________��
��3���жϵζ��յ�������ǣ�_________________________________________________��
(��).����ʱ,pH��12��NaOH��Һ100mL��Ҫʹ����pHΪ11��������仯���Բ��ƣ�
��4�������������ˮ��Ӧ��_________mL��
��5���������pH��10��NaOH��Һ��Ӧ��_________mL��
��6�������0.01mol/L HCl��Ӧ��_________mL��
���𰸡� ���� ƫ�� ƫС �������һ��NaOH��Һ�����Һ����ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ 900 1000 81.8
��������(��)(1)���ݼ�ʽ�ζ�����װҺǰӦ����װҺ�������ϴ��������ˮϴ�Ӽ�ʽ�ζ��ܣ�������ע��NaOH��Һ����0���̶������ϣ�������ˮϴ�Ӽ�ʽ�ζ��ܺ�Ӧ��Ҫ�ñ���Һ��ϴ���ʢٴ���ʽ�ζ���δ�ñ�������Һ��ϴ��ֱ��ע���NaOH��Һ����Һ��Ũ��ƫС�����V(��)ƫ����c(����)= 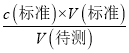 ����֪c(��)ƫ�ʴ�Ϊ���٣�ƫ��
����֪c(��)ƫ�ʴ�Ϊ���٣�ƫ��
(2)������У��ڼ��µζ���Һ�����ʱ���ζ��ܼ��������ݣ����V(��)ƫС������c(����)= 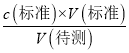 ����֪c(��)ƫС���ʴ�Ϊ��ƫС��
����֪c(��)ƫС���ʴ�Ϊ��ƫС��
(3)�ζ�ʱ������Һ��ɫ�仯�Ұ�����ڲ���ɫ����˵���ﵽ�ζ��յ㣬���Ե������һ��NaOH��Һ�����Һ����ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ���ʴ�Ϊ���������һ��NaOH��Һ�����Һ����ɫ��Ϊ��ɫ�Ұ�����ڲ���ɫ��
(��)(4)pH=12��NaOH��Һ������������Ũ����0.01mol/L��pH=11������������Һ������������Ũ����0.001mol/L�������ˮ�������V2��c1V1=c2(V1+V2)=0.01mol/L��0.1L=(0.1+V2)L��0.001mol/L����V2=![]() =0.9L=900mL���ʴ�Ϊ��900��
=0.9L=900mL���ʴ�Ϊ��900��
(5)pH=12��NaOH��Һ������������Ũ����0.01mol/L��pH=11������������Һ������������Ũ����0.001mol/L��pH=10������������Һ������������Ũ����0.0001mol/L�������pH=10��NaOH��Һ�����V2��c1V1+c2V2=c3(V1+V2)=0.01mol/L��0.1L+0.0001mol/L��V2=0.001mol/L(0.1+V2)����ã�V2=1L=1000mL���ʴ�Ϊ��1000��
(6)�����Ũ����0.01mol/L�����������������V��c(OH-)=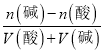 =
=![]() =0.001mol/L����ã�V=81.8mL���ʴ�Ϊ��81.8��
=0.001mol/L����ã�V=81.8mL���ʴ�Ϊ��81.8��


 Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д� ״Ԫ����ϵ�д�
״Ԫ����ϵ�д� ͬ������ϵ�д�
ͬ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���¶�Ϊ25��ʱ����0.23 g��Ͷ�뵽100gˮ�г�ַ�Ӧ�����跴Ӧ����Һ���Ϊ100mL�������Һ��pHΪ
A. 1 B. 13 C. 12 D. 10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ���������800��ʱ��Ӧ2NO(g)��O2(g) ![]() 2NO2(g)��ϵ����n(NO)��ʱ��ı仯���±���
2NO2(g)��ϵ����n(NO)��ʱ��ı仯���±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
��1��д���÷�Ӧ��ƽ�ⳣ������ʽ��K��__________��
��2��0��2 s�ڸ÷�Ӧ��ƽ������v(NO)��__________, v(O2)��__________��
��3����˵���÷�Ӧ�Ѵﵽƽ��״̬����__________��
a��v(NO2)��2v(O2)
b��������ѹǿ���ֲ���
c��v��(NO)��2v��(O2)
d���������ܶȱ��ֲ���
��4����ʹ�÷�Ӧ�ķ�Ӧ����������ƽ��������Ӧ�����ƶ�����__________��
a����ʱ�����NO2���塡�� b������O2��Ũ��
c������������� d��ѡ���Ч����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������Ϊһ�ֳ���ҩ�����н�����ʹ��Ч����ʵ�����Ʊ���������ʱ�������ñ���������������������������ȡ���������������ķ�Ӧ����Զ����������ᷴӦ�����ʣ���֪����������ˮ����������������ɫƬ״���壬�۵�114������������ˮ����������ˮ����������ˮ������Ӧ���������ѡ�ñ�����������Ϊԭ����ȡ���ᴿ�����������÷��ȷ�Ӧ��ԭ����
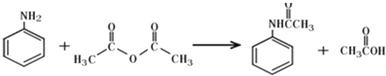
ʵ�鲽��
��ȡ5.0mL�������ܶ�1.04g/mL��������100mL��ƿ�У�����20mLˮ������ҡ�·�������6.0mL���������ܶ�1.08g/mL����������ȣ����н������������ò���������״�����飬�ٳ�ֽ��裻
�ڷ�Ӧ��ȫ��ʱ�ѷ�Ӧ�����ת�Ƶ��ձ��У���ȴ���ˣ�ϴ�ӣ��ô������������壻
�۽��ֲ�Ʒת����150mL�ձ��У���������ˮ���Ƴ�80���ı�����Һ���ټ������20%��ˮ������Ӱ����̿�������½���Һ���3��5min������������������ˮ��ϴ�ձ���©���еĹ��壬�ϲ���Һ����ȴ�ᾧ����������ϴ�ӡ����ɵ�����������Ʒ��
��1������������״�������������________________________________����Ӧ�¶ȹ��ᵼ�±����ӷ������п��Կ��Ʒ�Ӧ�¶ȣ���ֹ��Ӧ�¶����߹���IJ�����__��
A����Ӧ�����ʱ�ij�ֽ��� B����ҡ�·�������6.0mL������
C������������״������ D����20mLˮ
��2�������ϴ�Ӵֲ�Ʒʱ��ѡ�õ��ܼ���_______��
A����ˮ B����ˮ C��1��3���Ҵ���Һ D����Һ
��3������������õ����ˣ����й�����ѡ��________�����ˡ����ȹ��˻���ˣ���������������Ϊ�˳�ȥ_____________����������Һʱ����������ܼ���������___________��ѡ����ȷѡ���
A����ֹ���������У��ܼ���ʧ���ܲ����IJ�������
B����ֹ���������У��¶Ƚ��Ϳ��ܲ����IJ�������
C����ȥ����̿δ������ȫ����ɫ����
��4���������ȴ��Һʱ��ѡ��__��
A����ˮԡ��ȴ B��������ˮԡ��ȴ
C����������Ȼ��ȴ D��Ͷ�������������
��5���������������Щ����������߲���__________��
�����Ƴɱ�����Һ�������20%���ܼ����ڳ��ȹ��˽�����Һ���۹�����ʱ��������ˮ��ϴ�ձ���©���еĹ��壬�ϲ���Һ���ܼӻ���̿�������ݹ�����ʱ��ϴ��ѡ����ˮ������ˮϴ�ӹ��壮
A���٢ܢ� B���٢� C���ܢ� D���ڢܢ�
��6�����������ô�������������6.75g����֪������������������������Ħ�������ֱ�Ϊ93g/mol��102g/mol��135g/mol����ʵ��IJ���Ϊ________��������λ��Ч���֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Һ���Ƿ�����������������ѡ������Լ���
A.��ˮB.KMnO4��ҺC.KSCN��ҺD.Fe ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������m gij���壬����˫ԭ�ӷ��ӹ��ɣ�����Ħ������ΪM gmol��1 �� �������ӵ�������NA��ʾ����
��1������������ʵ���Ϊ��
��2������������ԭ������Ϊ����
��3���������ڱ�״���µ����Ϊ��
��4������������1Lˮ�У������Ƿ�Ӧ��������Һ�����ʵ���������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и�����ֵ���������У�������ˮ�ġ����ʵ������ı仯���仯����
A. ˮ�ķе㣻ˮ���ӵ���Ŀ B. ˮ��������ˮ����Է�������
C. ˮ�������ˮ������ԭ�ӵ���Ŀ D. ˮ���ܶȣ�ˮ��Ħ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��ˮ�ĵ���ﵽƽ�⣺H2OH++OH-��H��0������������ȷ���ǣ�������
A. ��ƽ����ϵ�м���ˮ��ƽ�������ƶ���c ��H+������
B. ��ˮ���ȣ�Kw����pH����
C. ��ˮ�м��������������ƹ��壬  ����
����
D. ��ˮ�м�������NaOH���壬ƽ�������ƶ���c��H+������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������CH3CH(CH3)CH(CH3)CH2CH(CH3)CH3�ǵ�ϩ��R��H2�����ӳɷ�Ӧ��IJ����R���ܵĽṹ�У� ��
A. 8�� B. 6�� C. 2�� D. 1��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com