
| A. | 氯水、氨水和食盐水都能导电,所以Cl2、NH3和NaCl都是电解质 | |
| B. | 向醋酸溶液中加入少量醋酸溶液,原醋酸电离平衡一定向右移动 | |
| C. | 升高温度能促进弱电解质的电离 | |
| D. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
分析 A、据电解质的概念分析;
B、向醋酸溶液中加入的醋酸溶液浓度比原醋酸溶液浓度大时,原醋酸溶液的电离平衡逆向移动;
C、弱电解质的电离吸热;
D、溶液导电能力的强弱决定于溶液中离子浓度的大小,与电解质的强弱无关.
解答 解:A、电解质是在水溶液或熔融状态下能够电离的化合物,Cl2和NH3都不是电解质,故A错误;
B、向醋酸溶液中加入的醋酸溶液浓度比原醋酸溶液浓度小时,相对于加水稀释,原醋酸溶液的电离平衡正向移动,故B错误;
C、电离吸热,升温能够促进弱电解质的电离,故C正确;
D、溶液导电能力的强弱决定于溶液中离子浓度的大小,与电解质的强弱无关,故D错误;
故选C.
点评 本题考查了电解质的判断、影响弱电解质电离平衡移动的因素、溶液导电能力强弱的影响因素,题目难度不大.


科目:高中化学 来源: 题型:选择题
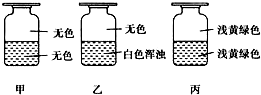 向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,现象如图所示,则甲、乙、丙注入的液体分别是( )
向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,现象如图所示,则甲、乙、丙注入的液体分别是( )| A. | ①②③ | B. | ②①③ | C. | ③②① | D. | ①③② |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+)+c(CH3COO-)+c(CH3COOH)=0.1mol/L | |
| B. | 加入少量0.1mol/L的盐酸,电离平衡向左移动,c(H+)减小 | |
| C. | 加入少量NaOH固体,电离平衡向右移动,溶液导电性增强 | |
| D. | 加入少量CH3COONa固体,电离平衡不移动,溶液导电性减弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
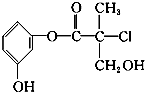
| A. | 该有机物的分子式为C10H11O4Cl | |
| B. | 该有机物与浓溴水可发生取代反应,且与浓硫酸混合共热可发生消去反应 | |
| C. | 1 mol该有机物与足量NaOH溶液反应最多消耗4 mol NaOH | |
| D. | 该有机物经催化氧化后与新制氢氧化铜悬浊液共热生成砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CuSO4变成CuSO4•5H2O是物理变化 | |
| B. | 一定条件下,新制的Cu(OH)2浊液能与乙醛反应但不能与乙酸反应 | |
| C. | CuO是黑色固体,与水反应可生成Cu(OH)2 | |
| D. | Cu2O遇硝酸可能会被氧化成Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com