
����Ŀ���״���һ�ֿ������������Դ��һ����������CO��H2�ϳ�CH3OH��CO��g��+2H2 ��g��CH3OH��g����H=a kJmol��1 �� �����Ϊ2L���ܱ������г���2mol CO��4mol H2 �� ��ò�ͬ�¶������������������ʵ�����ʱ�䣨min���ı仯��ϵ��ͼ�Т�������ʾ�� 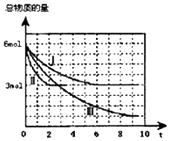
��1�����жϷ�Ӧ�ﵽ��ѧƽ��״̬����������ĸ����
A.c��CO����c��H2���ı�ֵ���ֲ���
B.����������ѹǿ���ֲ���
C.�����������ܶȱ��ֲ���
D.��λʱ������1molCO���ĵ�ͬʱ��1mol CH3OH����
E.v����H2��=2v����CH3OH��
��2���٢�͢���ȣ���ı�ķ�Ӧ������ ��
�ڷ�Ӧ����9minʱ�ﵽƽ�⣬�ȽϷ�Ӧ����¶ȣ�T1���ͷ�Ӧ����¶ȣ�T3���ĸߵͣ�T1T3���������������=������������Ӧ����Ӧ������Ȼ����ȡ�����
��3���ٷ�Ӧ����6minʱ�ﵽƽ�⣬�ӷ�Ӧ��ʼ���ﵽƽ��ʱv ��CH3OH��=mol/��Lmin����
�ڷ�Ӧ����2minʱ�ﵽƽ�⣬������¶��µ�ƽ�ⳣ��K= �� ��������¶Ȳ���������£���������Ӧ�ﵽƽ���ʱ�����������м���1mol CO��3mol CH3OH��ƽ�⽫���������Ӧ���淴Ӧ�Ͳ��ƶ�������ԭ���� ��
���𰸡�
��1��BE
��2��ʹ�ô�������������
��3��0.125��12�����ƶ�����Ϊƽ������1molCO��3molCH3OH����ʱ 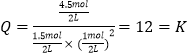 ������ƽ�ⲻ�ƶ�
������ƽ�ⲻ�ƶ�
���������⣺��1��A��c��CO����c��H2���ı�ֵ���ֲ���δ˵�����淴Ӧ������˵����Ӧ����ƽ�⣬�ʴ��� B���淴Ӧ���л���������ʵ�����С�����º�����ѹǿ��С��������ѹǿ���ֲ���˵������ƽ�⣬����ȷ�� C������������������䣬���º����£������������ܶ�ʼ�ձ��ֲ��䣬����˵����Ӧ����ƽ�⣬�ʴ��� D����λʱ������1molCO���ĵ�ͬʱ��1mol CH3OH����δ˵�����淴Ӧ������˵����Ӧ����ƽ�⣬�ʴ��� E��v����H2��=2v����CH3OH��˵�����淴Ӧ����������ȣ���˵����Ӧ����ƽ�⣬����ȷ����ѡBE����2���٢�͢���ȷ�Ӧ���ʼӿ죬��Ӱ��ƽ���ƶ�������ӦΪ�������ʵ�����С�ķ�Ӧ��Ӧ��ʹ�ô��������Դ��ǣ�ʹ�ô������ڷ�Ӧ���ƽ��ʱ���õ�ʱ��ȷ�Ӧ���ƽ��ʱ���õ�ʱ�䳤����ѧ��Ӧ�������������¶Ƚϵͣ���T1��T3 �� �����¶ȣ�����������ʵ������ӣ����������ƶ������Է�Ӧ�Ƿ��ȵģ����Դ��ǣ����� ���ȣ���3���ٷ�Ӧ����6minʱ�ﵽƽ�⣬�ӷ�Ӧ��ʼ���ﵽƽ��ʱv ��CH3OH��=mol/��Lmin����
CO��g��+ | 2H2 ��g�� | CH3OH��g�� | ��H=a kJmol��1 | |
��ʼ�� | 2mol | 4mol | 0 | |
�仯�� | x | 2x | x | |
ƽ���� | 2-x | 4-2x | x |
��2��x+4��2x+x=3�����x=1.5������v ��CH3OH��= ![]() mol/��Lmin��=0.125 mol/��L��min����
mol/��Lmin��=0.125 mol/��L��min����
���Դ��ǣ�0.125���ڢ��¶���ͬ��ƽ�ⳣ����ͬ��ƽ�ⳣ��K����= ![]() =
=  =12����ʱŨ����Qc=
=12����ʱŨ����Qc=  =12=K����ƽ�ⲻ�ƶ���
=12=K����ƽ�ⲻ�ƶ���
���Դ��ǣ�12�����ƶ��� ��Ϊƽ������1molCO��3molCH3OH����ʱ 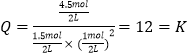 ������ƽ�ⲻ�ƶ���
������ƽ�ⲻ�ƶ���
�����㾫����������Ҫ�����˻�ѧƽ��״̬���ʼ������ͻ�ѧƽ��״̬���жϵ����֪ʶ�㣬��Ҫ���ջ�ѧƽ��״̬�����������ȡ��� V��=V��>0�����������Ƕ�̬ƽ�⣬ƽ��ʱ��Ӧ���ڽ��У�����������Ӧ������и���ְٷֺ������䣻���䡱�������ı䣬ƽ�ⱻ���ƣ������µ������½����µĻ�ѧƽ�⣻��;���أ�����������䣬���淴Ӧ�����Ǵ�����Ӧ��ʼ�����Ǵ��淴Ӧ��ʼ�����ɽ���ͬһƽ��״̬����Ч����״̬�жϣ���v(B��)=v(B��)��v(C��):v(D��)=x : y��c(C)��C%��n(C)%�Ȳ������A��B��C��DΪ���壬��m+n��x+y��ѹǿ�㶨����ϵ��ɫ�����λʱ����ij�����ڻ�ѧ���Ķ����������γ�������ϵƽ��ʽ���㶨��m+n �� x+y���Ȳ�����ȷ�����⣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʼ�ķ�Ӧ���������仯������ͼ��ʾ���ǣ� �� 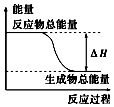
A.�������������ڼ��������µķ�Ӧ
B.���ȵ�̼�������̼��Ӧ
C.Ba��OH��28H2O�����NH4Cl������
D.̼��ˮ������������ȡˮú���ķ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��һ��Ӧ�ü���㷺�Ļ���ԭ�ϣ�������ij�����ú�����ͭΪԭ������������CuSO45H2O������������ʾ��ͼ�� 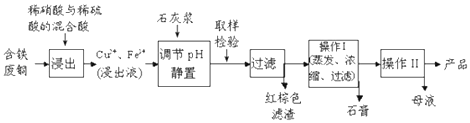
������ʯ���ڲ�ͬ�¶��µ��ܽ�ȣ�g/100gˮ��������
�¶ȣ��棩 | 20 | 40 | 60 | 80 | 100 |
ʯ�� | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
���� | 32 | 44.6 | 61.8 | 83.8 | 114 |
��ش��������⣺
��1������ɫ��������Ҫ�ɷ�����
��2��д��������������������ͭ�Ļ�ѧ����ʽ��
��3������I�IJ����¶�Ӧ�ÿ����������ң�
��4������Һ�з��������ͭ����IJ���IIӦΪϴ�ӡ����
��5����Ӧ�����е�NO����ѭ��ʹ�ã��Խ���һ����ѧ����ʽ��ʾNOת��ΪHNO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������5OOmL2mol/L�����ᣬ��Ҫ36.5%��Ũ����(�ܶ�ԼΪ1.2g��cm-3)�����Ϊ
A. 27.4mL B. 83.3mL C. 120mL D. ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������Ϊ10L���ܱ������У�1mol X��1mol Y���з�Ӧ��2X��g��+Y��g��Z��g������60s�ﵽƽ�⣬����0.3mol Z������˵����ȷ���ǣ� ��
A.0��60 s����X��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ0.001 molL��1s��1
B.�����������Ϊ20 L��Z��ƽ��Ũ�ȱ�Ϊԭ���� ![]()
C.������ѹǿ��������Y��ת���ʼ�С
D.�������¶ȣ�X���������������÷�Ӧ�ġ�H��0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ϊһ�����ʹ��ܵ�أ���Ӧ���õ����Ӻͷ�չ��
��1��Al��NO3��3���Ʊ������ز�����ԭ��֮һ������Al��NO3��3�������ջ����е�ˮ�֣������Ҫ������ж������������岽����ͼ��ʾ�� 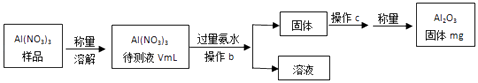
�ټ��������ˮ������Ӧ�����ӷ���ʽΪ�� ��
�ڲ���bΪ��
��Al��NO3��3����Һ�У�c��Al3+��=mol/L���ú�m��V�Ĵ���ʽ��ʾ����
��2�������������ڽ����ơ�������Ͷ����ƣ�Na2SX���ֱ���Ϊ�����缫�ķ�Ӧ�����Al2O3�մɣ��ɴ���Na+��Ϊ����ʣ��䷴Ӧԭ����ͼ1��ʾ�� 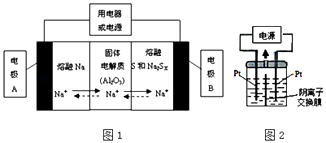
���� | Na | S | Al2O3 |
�۵�/�� | 97.8 | 115 | 2050�� |
�е�/�� | 892 | 444.6 | 2980 |
�ٸ��ݱ����ݣ������жϸõ�ع���������Ӧ������������ĸ����Χ�ڣ�
A.100������ B.100��300��C.300��350��D.350��2050��
�ڷŵ�ʱ���缫AΪ�����缫B������Ӧ���������ԭ����
�۳��ʱ���ܷ�ӦΪNa2SX�T2Na+xS��3��x��5�����������ĵ缫��ӦʽΪ�� ��
��3��������������Ϊ��Դ��������װ��KI��������Һ��ͼ2��ʾ�����ڵ��м��������ӽ���Ĥ������ͨ��һ��ʱ����������Һ����ɫ��һ��ʱ�����ɫ��dz�����Ҳ���ĵ缫����ʽ�����Է��������Һ��ɫ��dz�Ŀ���ԭ���ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����г������ʵ������뻯ѧʽ��Ӧ��ȷ����
A.ˮú��-CH4B.����-KAl(SO4)2��12H2O
C.ˮ����-H2SiO3D.����-NaHCO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��þ�����ֱ����Ũ�ȡ�������Ĺ���ϡ���ᷴӦ����������������V����ʱ�䣨t����ϵ��ͼ����Ӧ��þ�����Ĺ�ϵ˵����ȷ���ǣ�������
A.���ʵ���֮��Ϊ3��2
B.����֮��Ϊ3��4
C.Ħ������֮��Ϊ9��8
D.���֮��Ϊ2��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й������ǵ������У��������(����)
A. �ܼ���������Ԫ��B. �ܷ���������Ӧ
C. ���봼����������ӦD. �ܱ�����ΪCO2��H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com