
【题目】常温下,铝条与下列溶液不能持续反应的是( )
A.氢氧化钠溶液B.浓硫酸C.稀硫酸D.硫酸铜溶液
 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源: 题型:
【题目】下列物质中既能与强酸反应,又能与强碱反应,且都能生成盐和水的是( )
①Al ②Al2O3 ③Al(OH)3 ④Na2CO3
A.①③B.②③④C.②③D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
① Al2O3 ② Cu(OH)2 ③ Al(OH)3 ④ Na2CO3 ⑤ NaHCO3
A. ①②⑤ B. ②④ C. ①②④ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a g钠、铝的混合物,放入b g水中,反应停止后得到的沉淀有c g,则溶液中溶质为( )
A. NaOH B. NaAlO2 C. NaOH和NaAlO2 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
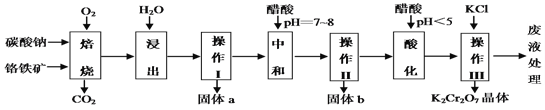
【题目】铬铁矿的主要成分可表示为FeO·Cr2O3,还含有MgO、Al2O3、Fe2O3等杂质,下图所示是以铬铁矿为原料制备重铬酸钾(K2Cr2O7)的工艺流程。
已知1:物质的溶解度(g/100g水)
物质 | 0℃ | 40℃ | 80℃ |
KCl | 28.0 | 40.1 | 51.3 |
NaCl | 35.7 | 36.4 | 38.0 |
K2Cr2O7 | 4.7 | 26.3 | 73.0 |
Na2Cr2O7 | 163.0 | 215.0 | 376.0 |
已知2:①焙烧时有Na2CrO4、 Fe2O3 、NaAlO2 等生成。
②Cr2O72- + H2O ![]() 2CrO42- + 2H+ ;
2CrO42- + 2H+ ;
③Cr2O72-具有很强的氧化性
回答问题:
(1)“浸出”步骤中,为了提高浸出率,可采取的措施有加热、研磨或_______________等(要求写一条)。
(2)固体b中主要含有______________________(填写化学式)。
(3)要检测酸化操作中溶液的pH是否等于4.5,应该使用_______(填写仪器或用品名称)。
(4)酸化步骤用醋酸调节溶液的pH﹤5,其目的是____________________;不用盐酸调节溶液pH的原因是______________________________________。
(5)操作III发生反应的化学方程式是____________________________ ;
(6)写出焙烧时生成NaAlO2的化学方程式____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知下列反应:①2Na+2H2O═2NaOH+H2↑ ②2F2+2H2O═4HF+O2③Cl2+H2O═HCl+HClO④2NaCl+2H2O ![]() 2NaOH+H2↑+Cl2↑⑤CaO+H2O═Ca(OH)2⑥CaCO3+H2O+CO2═Ca(HCO3)2
2NaOH+H2↑+Cl2↑⑤CaO+H2O═Ca(OH)2⑥CaCO3+H2O+CO2═Ca(HCO3)2
(1)其中水在反应中作氧化剂的反应是(填代号下同) .
(2)其中水在反应中作还原剂的反应是 .
(3)其中水在反应中既不作氧化剂也不作还原剂的反应是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知在稀溶液中,酸跟碱发生中和反应生成1 mol水时的反应热叫做中和热。现利用如图装置进行中和热的测定,请回答下列问题:

(1)图示装置有两处重要组成部分未画出,它们是____________ 、_______________。
(2)烧杯间填满碎泡沫塑料的作用是 ________________。
(3)若操作时分几次注入反应液,求得的反应热数值_____(填“偏大”“偏小”或“无影响”)。
(4)做一次完整的中和热测定实验,温度计需使用__________次。
(5)量取0.5 mol/L的盐酸和0.55 mol/L的NaOH溶液各50 mL进行实验,测得盐酸和NaOH溶液起始平均温度为t1℃,混合反应后最高温度为t2℃,设溶液密度均为1 g/mL,生成溶液的比热容c= 4.18 J/(g℃)。请列式计算中和热:△H= ______________kJ/mol(不用化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,科学家合成一系列具有独特化学特性的氢铝化合物(AlH3)n。已知,最简单的氢铝化合物Al2H6的球棍模型如下图所示,它的熔点为150 ℃,燃烧热极高。下列说法肯定错误的是( )

A. Al2H6在固态时所形成的晶体是分子晶体
B. Al2H6在空气中完全燃烧,产物为氧化铝和水
C. 氢铝化合物可能成为未来的储氢材料和火箭燃料
D. 氢铝化合物中可能存在组成为AlnH2n+2的一系列物质(n为正整数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com