

 ����A��B�ķ�Ӧ�����ǣ���ԭ��Ӧ��
����A��B�ķ�Ӧ�����ǣ���ԭ��Ӧ�� ��
�� Ϊԭ���Ʊ�������X��
Ϊԭ���Ʊ�������X�� �����ṹ��ʽ��ͼ���ĺϳ�·������ͼ�����Լ�����ѡ�����ϳ�·������ͼʾ�����£�
�����ṹ��ʽ��ͼ���ĺϳ�·������ͼ�����Լ�����ѡ�����ϳ�·������ͼʾ�����£� ��
�� ���� �Ա�A��C�Ľṹ��ʽ��֪BΪ ��B��SOCl2����ȡ����Ӧ����
��B��SOCl2����ȡ����Ӧ���� ��Ȼ����NaCN����ȡ����Ӧ����
��Ȼ����NaCN����ȡ����Ӧ���� ����ˮ�⡢��ԭ����������
����ˮ�⡢��ԭ���������� ����
���� �Ʊ�
�Ʊ� ������Ũ��������������
������Ũ�������������� ��Ȼ����HCl�����ӳɷ�Ӧ����
��Ȼ����HCl�����ӳɷ�Ӧ����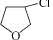 ����NaCN����ȡ����Ӧ����
����NaCN����ȡ����Ӧ����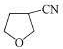 ���ڴ���������������Ӧ������
���ڴ���������������Ӧ������ ���ݴ˴��⣮
���ݴ˴��⣮
��� �⣺�Ա�A��C�Ľṹ��ʽ��֪BΪ ��B��SOCl2����ȡ����Ӧ����
��B��SOCl2����ȡ����Ӧ���� ��Ȼ����NaCN����ȡ����Ӧ����
��Ȼ����NaCN����ȡ����Ӧ���� ����ˮ�⡢��ԭ����������
����ˮ�⡢��ԭ���������� ����
���� �Ʊ�
�Ʊ� ������Ũ��������������
������Ũ�������������� ��Ȼ����HCl�����ӳɷ�Ӧ����
��Ȼ����HCl�����ӳɷ�Ӧ���� ����NaCN����ȡ����Ӧ����
����NaCN����ȡ����Ӧ���� ���ڴ���������������Ӧ������
���ڴ���������������Ӧ������ ��
��
��1���ɽṹ��ʽ��֪C���еĹ�����Ϊ�Ѽ�����ԭ�ӣ�
�ʴ�Ϊ���Ѽ�����ԭ�ӣ�
��2��BΪ ���Ƚ�A��B�Ľṹ��֪����A��B�ķ�Ӧ�ǽ�A�е�ȩ����ԭΪB�е��ǻ������Է�Ӧ�����ǻ�ԭ��Ӧ��
���Ƚ�A��B�Ľṹ��֪����A��B�ķ�Ӧ�ǽ�A�е�ȩ����ԭΪB�е��ǻ������Է�Ӧ�����ǻ�ԭ��Ӧ��
�ʴ�Ϊ�� ����ԭ��Ӧ��
����ԭ��Ӧ��
��3�����������ٷ��Ӻ���2��������������������״�ṹ�����ܷ���������Ӧ��ˮ�ⷴӦ��˵����ȩ�����������۲��ܺ�FeCl3������ɫ��Ӧ����ˮ�������ԣ�˵��û�з��ǻ���ˮ���������ǻ�����������м�������Ľṹ�������к��м������A�Ľṹ��ʽ��֪��ͬ���칹��Ϊ�����������������ţ��ֱ�Ϊ-OH��-CH3�����������ݶ�����һ��ԭ����10�ֽṹ�������������������ֱ������������-OH��-CH3�����������Ľṹ��9�֣����о�����������ֱ����������-OOCCH3��������3�֣����Թ���22�֣����з�����ֻ����6�ֵ�Ч��Ľṹ��ʽΪ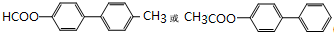 ��
��
�ʴ�Ϊ��22��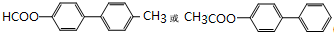 ��
��
��3��E��һ��ͬ���칹�庬��3�ֲ�ͬ��ѧ�������⣬�Һ���2���������ҽṹ�Գƣ����Ӧ�Ľṹ�� ��
��
�ʴ�Ϊ�� ��
��
��4���� �Ʊ�
�Ʊ� ������Ũ��������������
������Ũ�������������� ��Ȼ����HCl�����ӳɷ�Ӧ����
��Ȼ����HCl�����ӳɷ�Ӧ���� ����NaCN����ȡ����Ӧ����
����NaCN����ȡ����Ӧ���� ���ڴ���������������Ӧ������
���ڴ���������������Ӧ������ ��Ҳ����HCl��Ӧ����
��Ҳ����HCl��Ӧ����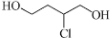 ��������
�������� ��
��
������Ϊ ��
��
�ʴ�Ϊ�� ��
��
���� �����漰�л���ĺϳɣ�������ѧ���ķ��������Ŀ��飬����ʱע����������Ϣ�Լ������ŵ����ʣ�ע��ϳ�·�ߵ���ƣ�Ϊ��������ѵ㣬��Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na3N��ˮ�ķ�Ӧ��������ԭ��Ӧ | |
| B�� | Na3N �ǹ��ۻ����� | |
| C�� | Na3N��4�����Ӿ����������8�����ȶ��ṹ | |
| D�� | Na3N�������Ӱ뾶���ڵ����Ӱ뾶 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�����м������������ƹ������������ĵ���̶� | |
| B�� | 25��ʱ���������Ũ�ȵ������백ˮ��Ϻ���Һ������ | |
| C�� | 25��ʱ��0.1mol•L-1��������Һ�ȵ�Ũ�ȵ�������Һ�ĵ��������� | |
| D�� | FeCl3��MnO2���ɼӿ�H2O2�ֽ⣬ͬ�������¶��߶�H2O2�ֽ����ʵĸı���ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ��֪ͼ������ϵFe3+��aq��+SCN-��aq��?Fe��SCN��2+��aq�� �е�c[Fe��SCN��2+]�¶�T��ƽ��ͼ��A����B����ȣ�A���c��Fe3+�� �� | |
| B�� | ͼ�ڱ�ʾþ�����ֱ����Ũ�ȡ�������Ĺ���ϡ���ᷴӦ��������������V ��ʱ��t�Ĺ�ϵ����Ӧ��þ�����ķ�Ӧ����֮��Ϊ2��3 | |
| C�� | ͼ�۱�ʾ��ԴX��Ϊ������U�ι���ΪAgNO3��Һ����b���е缫��Ӧʽ�ǣ�4OH--4e-=O2��+2H2O | |
| D�� | ͼ�ܱ�ʾ����CCl4��ȡ��ˮ���ѷֲ���л����ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.35g | B�� | 0.27g | C�� | 0.54g | D�� | 2.7g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 18y/x | B�� | 9y/x | C�� | 18y/x mol-1 | D�� | 9y/x mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ʵ������Ũ������MnO2��Ӧ��Cl2��MnO2+4HCl��Ũ��$\frac{\underline{\;��\;}}{\;}$Cl2��+Mn2++2Cl-+2H2O | |
| B�� | ��Ba��OH��2��Һ����μ���NH4HSO4��Һ��Ba2+�պó�����ȫ��Ba2++2OH-+H++${SO}_{4}^{2-}$+${NH}_{4}^{+}$�TBaSO4��+NH3•H2O+H2O | |
| C�� | ��NaOH��Һ�еμ�ͬŨ�ȵ�����Ca��HCO3��2��Һ��Ca2++${HCO}_{3}^{-}$+OH-�TCaCO3��+H2O | |
| D�� | ����״����112mL����ͨ��10mL��1 mol/L���廯������Һ�У�2Br-+Cl2�T2Cl-+Br2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com