

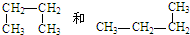 ⑧
⑧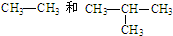
 的组成与结构都相同,属于同一物质;
的组成与结构都相同,属于同一物质;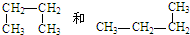 的组成与结构都相同,属于同一物质;
的组成与结构都相同,属于同一物质;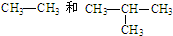 都属于烷烃,结构相差,生成2个CH2原子团,互为同系物;
都属于烷烃,结构相差,生成2个CH2原子团,互为同系物;

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、1mol Na2O2晶体中含有的离子总数为2NA |
| B、常温常压下,32g臭氧与氧气混合物中,含有2NA个氧原子 |
| C、假设1mol氯化铁完全转化为氢氧化铁胶体,则分散系中胶粒微粒数为NA |
| D、1mol Na2O2与足量的CO2反应,转移的电子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素 | 甲 | 乙 | 丙 | 丁 |
| 原子半径/nm | 0.186 | 0.102 | 0.152 | 0.074 |
| 主要化合价 | +1 | +6、-2 | +1 | -2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
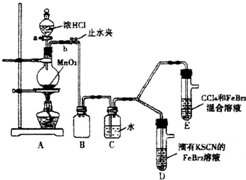 某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验
某化学兴趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入 适量浓盐酸;然后关闭活塞a, 点燃酒精灯 |
D装置中:溶液变红 E装置中:水层溶液变黄,振荡后CCl4层无明显变化 |
通过该实验现象,氧化性强弱的结论为: |
| I.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2 Ⅱ.Cl2和Br2反应生成BrCl,它呈红色,遇水迅速发生水解,也可发生反应:BrCl+KBr═KCl+Br2 Ⅲ.AgClO、AgBrO均可溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 的沸点比
的沸点比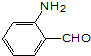 高,原因是
高,原因是查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、6.72L | B、8.96L |
| C、4.48L | D、5.6L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com