
【题目】某同学用下列所示实验装置制取乙酸乙酯.回答以下问题: 
(1)在大试管中先加入3mL , 然后一边摇动一边慢慢地加入2mL和2mL乙酸,混合均匀,然后加入几粒碎瓷片.按上图连好装置,用酒精灯对大试管小心均匀加热.当观察到明显现象时停止实验.
(2)与书中采用的实验装置的不同之处是:这位同学采用了球形干燥管代替了长导管,并将干燥管的末端插入了饱和碳酸钠溶液中.在此处球形干燥管的作用除了使乙酸乙醋充分冷凝外还有;
(3)有甲、乙、丙三位同学,分别将乙酸与乙醉反应得到的酯(未用饱和Na2CO3溶液承接)提纯,在未用指示剂的情况下,他们都是先加NaOH中和过量的酸,然后用蒸馏法将酯分离出来.但他们的结果却不同: ①甲得到了不溶于水的中性酯;②乙得到显酸性的酯的混合物;③丙得到大量水溶性物质.
试判断三位同学加入的NaOH是多了还是怡好还是少了(填“少量”、“适量”、“过量“)
①②③
【答案】
(1)乙醇;浓H2SO4
(2)防倒吸
(3)适量;少量;过量
【解析】解:(1)乙醇、乙酸在浓硫酸做催化剂,吸水剂条件下加热反应生成乙酸乙酯,浓硫酸密度大,稀释时放出大量的热,所以应将浓硫酸加入到乙醇中,以防酸液飞溅,乙酸易挥发,冷却后再加入乙酸;添加顺序依次乙醇、浓硫酸、乙酸;所以答案是:乙醇 浓H2SO4;(2)乙酸和乙醇易溶于水,不插入液面下是为了防止倒吸,球形干燥管导气的同时也起到防倒吸作用,
所以答案是:防倒吸;(3)①甲得到了不溶于水的中性酯,没有酸,说明所加NaOH溶液恰好中和了过量的酸,
所以答案是:适量;②乙得到显酸性的酯的混合物,酸有剩余,说明是所加NaOH溶液不足未将酸完全反应,
所以答案是:少量;③丙得到大量水溶性物质,说明没有酯,是因为所加NaOH溶液过量,酯发生水解,
所以答案是:过量.


 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源: 题型:
【题目】A、B、C是单质,其中A是金属,各种物质间的转化关系如图:

根据图示转化关系回答:
(1)写出下列物质的化学式:
A______________,B___________,乙__________,丁_________;
(2)写出下列变化的化学方程式:
①A与NaOH溶液反应的化学方程式____________________________________;
②甲与NaOH溶液反应的离子方程式____________________________________;
(3)将一定量的A加入到NaOH溶液中,产生的C在标准状况下的体积为3.36 L,则消耗的A的物质的量为________,转移电子数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是常见物质间的转化关系.其中甲、乙、丙均为非金属单质;A、B、E和丁均为化合物;B和E为能产生温室效应的气体且1mol E中含有 10mol电子.乙和丁为黑色固体,将它们混和加热后发现固体由黑色变为红色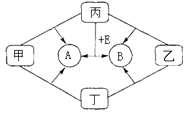
(1)写出化学式:甲;乙;丙;
(2)丁的摩尔质量为 .
(3)写出丙和E反应生成A和B的化学方程式:
(4)有学生将乙和丁混和加热后收集到标准状况下气体8.96L,测得该气体对氢气的相对密度为16,若将气体通入足量的澄清石灰水中,得到白色沉淀物g.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Mg2+、NH4+、Al3+混合溶液中加入Na2O2的量与生成沉淀和气体的量(纵坐标)的关系如图所示,则溶液中三种离子的物质的量之比为( ) 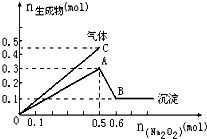
A.2:1:2
B.1:2:2
C.2:2:1
D.9:2:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列液体中,滴入水中出现分层现象,滴入热的氢氧化钠溶液中分层现象不会逐渐消失的是(不考虑有机物的挥发)( )
A.溴乙烷B.乙醛C.橄榄油D.汽油
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁是人类较早使用的金属之一.运用铁及其化合物的知识,完成下列问题.
(1)所含铁元素既有氧化性又有还原性的物质是______(用字母代号填).
A.FeB.FeCl3C.FeSO4D.Fe2O3
(2)向沸水中逐滴滴加1mol/LFeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是______nm.
(3)检验溶液中Fe3+存在的试剂是______(填物质名称),证明Fe3+存在的现象是______.电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:______.
(4)若要验证溶液中不含Fe3+而只含有Fe2+,正确的实验操作方法及现象是______.
(5)欲从制造印刷电路板的废水中回收铜,并重新获得FeCl3溶液设计实验方案如下:
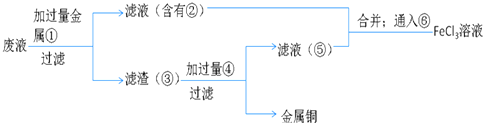
A.请写出上述实验中加入或生成的有关物质的化学式:
①______④______
B.请写出通入⑥反应的离子方程式______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化铁胶体制备步骤如下:
①用烧杯取少量蒸馏水,放在酒精灯上加热至沸腾;
②向烧杯中逐滴加入饱和FeCl3溶液;
③继续煮沸至液体是透明的红褐色,即得Fe(OH)3胶体.
回答下列问题:
(1)写出制备Fe(OH)3胶体的化学方程式;
(2)如何确定你制备胶体是否成功?;
(3)若向Fe(OH)3胶体中逐滴加入H2SO4溶液至过量会出现的现象: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中氧原子数目与6.8gH2O2中氧原子数目一定相等的是( )
A.6.72L CO
B.6.6gCO2
C.8gSO3
D.9.8gH2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】教材中给出了Na2O2与水反应的化学方程式,某学习小组通过实验研究Na2O2与水发反应机理
操作 | 现象 |
Ⅰ.向盛有4.0gNa2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生的气体能使带火星木条复燃,固体全部溶解后,得到的无色溶液a |
Ⅱ.向溶液a中滴入两滴酚酞 | 溶液变红,10分钟后溶液颜色明显变浅,稍后,溶液变为无色 |
Ⅲ.向溶液中加入少量MnO2粉末 | 又有大量气泡产生,产生的气体也能使带火星木条复燃 |
(1)Na2O2的电子式为 , 很明显,实验证实了溶液a中H2O2的存在,应用同位素示踪原理可以表示反应的机理,写出Na218O2与H2O反应的化学方程式 .
(2)操作Ⅱ中红色褪去的可能原因是 .
(3)用反应2MnO4﹣+5H2O2+6H+=2Mn2++502↑+8H2O测定溶液a中H2O2含量.取20.00mL溶液a,用稀(填化学式)酸化,用0.002molL﹣1KMnO4溶液滴定,至终点时平均消耗10.00mLKMnO4溶液.滴定时KMnO4溶液应装在(填酸或碱)式滴定管中,终点确定的方法是 , 经计算溶液a中c(H2O2)=molL﹣1
(4)向溶液a中滴加FeSO4溶液,发生反应的离子方程式为 .
(5)向FeSO4溶液中加入一定量Na202固体,并以物质的量为2:1发生反应,反应中无气体生成,写出反应的离子方程式 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com