
【题目】下列溶液一定是碱性的是 ( )
A. pH = 8的某电解质溶液 B. c(OH-)>1×10-7mol/L
C. 溶液中含有OH-. D. 溶液中c(OH-)>c(H+)
科目:高中化学 来源: 题型:
【题目】某温度时,N2与H2反应过程中的能量变化如图所示。下列叙述正确的是

A.a曲线是加入催化剂时的能量变化曲线
B.在密闭容器中加入1 mol N2、3 mol H2,充分反应放出的热量小于92 kJ
C.由图可知,断开1mol 氮氮三键与1 mol 氢氢键吸收的能量和小于形成1mol 氮氢键所放出的能量
D.反应物的总能量低于生成物的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关离子方程式,正确的是
A.稀硝酸和过量的铁屑反应:Fe+4H++NO3-=Fe3++NO↑+2H2O
B.NH4HCO3溶液与足量的NaOH溶液混合加热:NH4++HCO3-+2OH-![]() NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
C.碳酸氢钠溶液水解的离子方程式:HCO3-+H2O![]() CO32-+H3O+
CO32-+H3O+
D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于元素性质和结构的递变情况的说法错误的是( )
A. Li、Be、B原子最外层电子数依次增多
B. P、S、Cl元素最高正价依次升高
C. N、O、F原子半径依次增大
D. Na、K、Rb的电子层数逐渐增多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cl2是一种重要的化工原料,下图是一些含氯产品:

(1)①中钢瓶上应贴的标签为________。
A.腐蚀品 B.爆炸品 C.有毒品 D.易燃品
(2)84消毒液是一种无色、有漂白作用的液体,它的有效成分是________。
A.NaOH B.NaClO C.KMnO4 D.Na2O2
(3)Cl2可用于制盐酸,其化学方程式为______________________________________。
(4)工业上制漂白粉的化学方程式为________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚合硫酸铁(PFS)是水处理中重要的絮凝剂,以废铁屑为原料制备PFS的具体工艺流程如下:
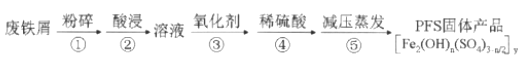
下列说法不正确的是( )
A. 步骤①,粉碎的目的是增大反应物接触面积,提高“酸浸”反应速率
B. 步骤③,可选用H2O2、Cl2、KMnO4等氧化剂将Fe2+转化为Fe3+
C. 步骤④,加稀硫酸调节pH在一定范围内,若pH偏小则Fe3+水解程度太弱,若pH偏大时则形成Fe(OH)3沉淀
D. 步骤⑤,减压蒸发,有利于降低蒸发温度防止产物分解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出由甲苯制备TNT的化学反应方程式_____________________;
(2)下图是8种环状的烃类物质:

①互为同系物的有__________和__________ (填名称,下同);互为同分异构体的有__________和__________、__________和__________;
②棱晶烷的二氯取代产物有__________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 实验室用盐酸酸化高锰酸钾溶液
B. 铁制或铝制容器可以盛装热的浓硫酸
C. 常温下,所有吸热反应都不能自发进行
D. 除去MgCl2溶液中少量FeCl3杂质,可加入足量的MgO粉末搅拌后过滤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为:
C(s)+H2O(g)![]() CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
能使化学反应速率加快的措施有________(填序号)。
①增加C的物质的量 ②升高反应温度
③随时吸收CO、H2转化为CH3OH ④密闭定容容器中充入CO(g)
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如下两组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
2 | 900 | 2 | 4 | 0.8 | 3.2 | 3 |
①实验1中以v(CO2)表示的化学反应速率为________。
②该反应的逆反应为________(填“吸”或“放”)热反应。
(3)在一容积为2 L的密闭容器内加入2 mol的CO和6 mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g) ![]() CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) ΔH<0,该反应的逆反应速率与时间的关系如图所示:
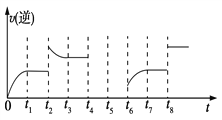
①由图可知反应在t1、t3、t7时都达到了平衡,而在t2、t8时都改变了条件,试判断t8时改变的条件可能是________。
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线。________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com