
分析 (1)化学平衡常数指在一定温度下,可逆反应达到平衡时,各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值;
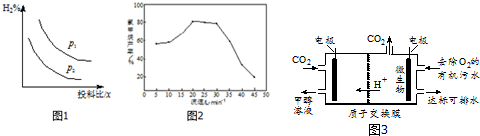
正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,氢气的含量降低;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式,反应热也进行相应的计算;
当△G=△H-T△S<0,反应可以自发进行;
流速过高反应物与催化剂的接触时间过短,原料利用率降低;
主、副反应中都有水生成,对主、副反应有抑制作用,提高CH3Cl纯度的同时,也降低了其产率;
(3)阴极发生还原反应,由电解池图结构可知,二氧化碳获得电子,在氢离子参与反应条件下生成甲醇.
解答 解:(1)可逆反应:CO(g)+2H2(g)?CH3OH(g),其平衡常数表达式K=$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;
由图可知,压强P1时的百分含量大于压强P2的百分含量,由于正反应为气体体积减小的反应,增大压强,平衡向正反应方向移动,氢气的含量降低,故压强P1<P2,
故答案为:$\frac{c(C{H}_{3}OH)}{c(CO)×{c}^{2}({H}_{2})}$;<;
(2)已知:①NH4Cl(s)=NH3(g)+HCl(g)△H=+163.9kJ•mol-1
②HCl(g)+CH3OH(g)→CH3Cl(g)+H2O(g)△H=-31.9kJ•mol-1
根据盖斯定律,①+②可得:NH4Cl(s)+CH3OH(g)→NH3(g)+CH3Cl(g)+H2O(g)△H=+132kJ•mol-1;
当△G=△H-T△S<0,正反应为吸热反应,由于反应△S>0,再高温下可以自发进行;
流流速过高反应物与催化剂的接触时间过短,原料利用率降低,导致产率降低;
主、副反应中都有水生成,对主、副反应有抑制作用,提高CH3Cl纯度的同时,也降低了其产率;
故答案为:NH4Cl(s)+CH3OH(g)→NH3(g)+CH3Cl(g)+H2O(g)△H=+132kJ•mol-1;△S>0;流速过高反应物与催化剂的接触时间过短,原料利用率降低,导致产率降低;对主副反应有抑制作用,提高CH3Cl纯度的同时,也降低了其产率;
(3)阴极发生还原反应,由电解池图结构可知,二氧化碳获得电子,在氢离子参与反应条件下生成甲醇,阴极电极反应式为:CO2+6H++6e-=CH3OH+H2O,
故答案为:CO2+6H++6e-=CH3OH+H2O.
点评 本题考查化学平衡常数含义及影响因素、热化学方程式的书写、可逆反应条件控制、电极反应式书写等,侧重考查学生对知识的迁移应用,难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cs+离子核间距为a cm,氯化铯的摩尔质量为M,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )| A. | $\frac{8M}{{N}_{A}•{a}^{3}}$g.cm-3 | B. | $\frac{M{a}^{3}}{8{N}_{A}}$gcm-3 | C. | $\frac{M}{{N}_{A}•{a}^{3}}$g.cm-3 | D. | $\frac{Ma}{{N}_{A}}$g.cm |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向淀粉水解液中滴加碘水,检验淀粉是否已经水解 | |
| B. | 利用多次滴加Na2SO4溶液能够提纯蛋白质 | |
| C. | 加新制Cu(OH)2悬浊液加热,可检验糖尿病人尿液中的葡萄糖 | |
| D. | 除去甲苯中含有的少量苯酚,可加入NaOH溶液振荡后,静置分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 氮分子的电子式 N:::N | B. | 镁原子的原子结构示意图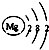 | ||
| C. | 质量数是16的氧原子 ${\;}_{8}^{16}O$ | D. | 乙醇的结构简式 C2H5OH |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:填空题

| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀(pH) | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀(pH) | 4.1 | 9.7 | 9.2 | 5.2 |
 H2O(l)═H+ (aq)+OH- (aq)△H=b kJ/mol
H2O(l)═H+ (aq)+OH- (aq)△H=b kJ/mol查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 离子 | Fe2+ | Fe3+ | Cu2+ |
| 开始沉淀时的pH(初始浓度为1.0mol/L) | 6.5 | 1.5 | 4.2 |
| 沉淀完全时的pH | 9.7 | 3.2 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 原子半径:A<B | |
| B. | 原子序数:A<B | |
| C. | 元素所在的周期数:A>B | |
| D. | A的最高正价与B的最低负价的绝对值一定相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com