
| A、35g |
| B、30 g |
| C、20 g |
| D、15 g |
 应用题作业本系列答案
应用题作业本系列答案 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
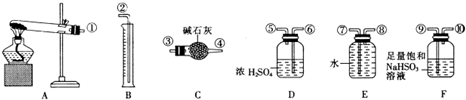
| 实验小组 | 称取硫酸铜的质量(g) | 装置c增加的质量(g) | 量筒中谁的体积折算成标准状况下气体的体积(mL) |
| 一 | 6.4 | 2.56 | 448 |
| 二 | 6.4 | 3.84 | 224 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2 mol |
| B、1.2 mol |
| C、0.1mol |
| D、1.6 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、应准确称取氢氧化钠固体19.2g |
| B、为了减少损失,将氢氧化钠固体直接倒入容量瓶中,加水溶解 |
| C、定容时仰视读数,所配制的溶液浓度会偏低 |
| D、摇匀后溶液液面低于刻度线,应补充适量蒸馏水至刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
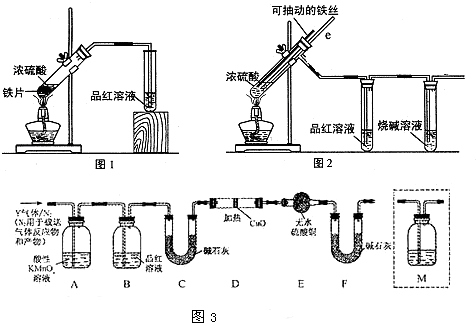
查看答案和解析>>
科目:高中化学 来源: 题型:
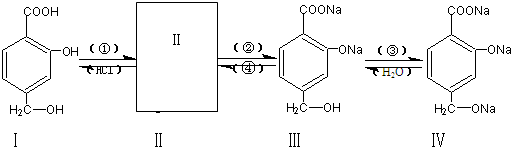
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、若M1>M2,平衡右移,△H<0 |
| B、若M1<M2,平衡右移,△H>0 |
| C、若M1>M2,平衡左移,△H>0 |
| D、若M1<M2,平衡左移,△H<0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com