

| A. | 灼烧操作在蒸发皿中进行 | |
| B. | 若X为烧碱,则Z为氨气,沉淀a为红棕色,可作颜料 | |
| C. | 若X为盐酸,则Z为CO2,溶液丙只含NaCl和Na2CO3 | |
| D. | 图示所发生的反应类型有:分解反应、复分解反应、氧化还原反应 |
分析 Al2O3、SiO2可与强碱反应,Al2O3、Fe2O3可与酸反应,如X为烧碱,则a为Fe2O3,溶液甲为NaAlO2和Na2SiO3,Y盐酸或稀硫酸,沉淀b为H2SiO3,溶液乙含有AlCl3,Z为氨水,沉淀c为Al(OH)3,丙为氯化铵、硫酸铵等;
若X为盐酸,a为SiO2,甲含有AlCl3、FeCl3,Y为NaOH,b为Fe(OH)3,溶液乙为NaAlO2,Z为CO2,c为Al(OH)3,丙为NaCl和NaHCO3,以此解答该题.
解答 解:Al2O3、SiO2可与强碱反应,Al2O3、Fe2O3可与酸反应,如X为烧碱,则a为Fe2O3,溶液甲为NaAlO2和Na2SiO3,Y盐酸或稀硫酸,沉淀b为H2SiO3,溶液乙含有AlCl3,Z为氨水,沉淀c为Al(OH)3,丙为氯化铵、硫酸铵等;
若X为盐酸,a为SiO2,甲含有AlCl3、FeCl3,Y为NaOH,b为Fe(OH)3,溶液乙为NaAlO2,Z为CO2,c为Al(OH)3,丙为NaCl和NaHCO3,
A.灼烧固体应在坩埚中进行,故A错误;
B.由以上分析可知,若X为烧碱,则Z为氨气,沉淀a为Fe2O3,为红棕色,可作颜料,故B正确;
C.由以上分析可知,若X为盐酸,则Z为CO2,溶液丙只含NaCl和NaHCO3,故C错误;
D.氢氧化铝生成氧化铝为分解反应,电解氧化铝生成铝的反应为氧化还原反应,其它为复分解反应,故D正确.
故选AC.
点评 本题考查化学工艺流程、无机物推断等,题目难度中等,理解工艺流程是解题的关键,需要学生基本扎实的据此与运用知识分析解决问题的能力.注意把握制备原理,把握物质的性质以及相关反应方程式的书写.该题侧重考查铝、硅、钠及其化合物的性质.


科目:高中化学 来源: 题型:解答题
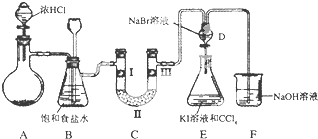
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 碱石灰 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用酸性KMnO4溶液将Fe2+氧化成Fe3+,再转化为Fe(OH)3沉淀除去 | |
| B. | 用ZnO调节浸出液的酸碱性,可使某些离子形成氢氧化物沉淀 | |
| C. | 在实际生产过程中,加入Ag2SO4可除去Cl-,是利用了沉淀转化的原理 | |
| D. | 也可以用ZnCO3代替ZnO调节溶液的酸碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若t℃时,0.05mol•L-1的Ba(OH)2溶液pH=11,t=25℃ | |
| B. | 常温下,向pH=a的醋酸溶液中加入等体积等浓度的硫酸后,pH=a+1 | |
| C. | 常温下,若c1mol•L-1的氨水与c2mol•L-1的盐酸等体积混合pH=7,则c1>c2 | |
| D. | 等体积等pH的CH3COOH溶液、盐酸分别与足量铝粉反应,盐酸生成H2的量更多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ca2+ | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有$S{O}_{4}^{2-}$ | |
| C. | 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ | |
| D. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中溶液变浑浊,一定有$C{O}_{3}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
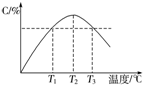
| A. | 0~5 min,C物质的平均反应速率为0.04 mol•L-1•min-1 | |
| B. | 图中温度T1时的正反应速率等于温度T3时的正反应速率 | |
| C. | 该反应温度T2时的平衡常数大于温度T3时的平衡常数 | |
| D. | 图中T2时,若只增大压强,则正、逆反应速率不改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 利用电泳现象区别溶液和胶体 | |
| B. | 用渗析的方法除去胶体中的离子或分子,以净化胶体 | |
| C. | 用滤纸过滤除去溶液中的胶体粒子 | |
| D. | 向新制Fe(OH)3胶体中加入足量AgNO3溶液,以除去胶体中的Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
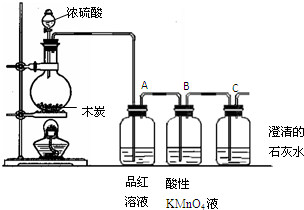
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③ | B. | ①② | C. | ①④ | D. | ①②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com