
| A. | 化学性质稳定 | B. | 还原性很强 | ||
| C. | 不与O3反应 | D. | 易与O2形成致密的氧化膜 |
 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 16g16O2和18O2的混合物中含有的质子数目为8NA | |
| C. | 电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子 | |
| D. | 取50ml14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 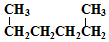 1,4-二甲基丁烷 1,4-二甲基丁烷 | B. | 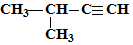 2-甲基-3-丁炔 2-甲基-3-丁炔 | ||
| C. |  2-丁醇 2-丁醇 | D. | CH2Cl-CH2Cl 二氯乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②④⑤ | C. | ①③④ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
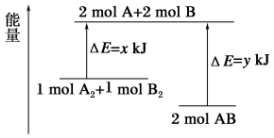
| A. | 该反应是吸热反应 | |
| B. | 断裂1molA-A键和1molB-B键可放出X kJ的能量 | |
| C. | 2molAB的总能量高于1molA2和1molB2的总能量 | |
| D. | 断裂2molA-B键需吸收YKJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质沸点随原子序数的递增而升高 | |
| B. | 周期表第一列是第ⅠA 族元素,又称碱金属元素 | |
| C. | 金属锂常用于制造锂电池,这跟它还原性强、密度小有关 | |
| D. | 金属锂在空气中燃烧,产物是 Li2O2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com