
分析 根据增大浓度、增大压强、使用催化剂,反应速率加快,反之反应速率减慢来解答,注意反应体系中各物质的浓度不变,则反应速率不变.
解答 解:①升高温度,反应速率增大,故答案为:增大;
②加入催化剂,反应速率增大,故答案为:增大;
③再充入H2,反应物浓度增大,化学反应速率增大,故答案为:增大;
④容器中压强不变,充入氖气,则容器容积扩大,相当于减小压强,则反应速率减小,故答案为:减小;
⑤容器容积不变,通入氖气,反应体系中各物质的浓度不变,则反应速率不变,故答案为:不变;
⑥保持压强不变,充入2x mol H2(g)和2y mol I2(g),各物质的浓度保持不变,所以速率不变,故答案为:不变.
点评 本题考查影响化学反应速率的因素,题目较简单,明确常见的影响因素即可解答.


科目:高中化学 来源: 题型:选择题
| A. | 只有① | B. | ③和④ | C. | ②和③ | D. | 只有③ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 化学键 | C═O(CO2) | C═O(COS) | C═S | H-S | H-O |
| E(kJ/mol) | 803 | 742 | 577 | 339 | 465 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用C表示该反应的速率为0.03mol/(L•s) | |
| B. | 达到平衡,测得放出热量为x kJ,则x=Q | |
| C. | 若向容器中再充入1 mol C,重新达到平衡,A的体积分数保持不变 | |
| D. | 若升高温度,则V (逆)增大,V(正)减小,平衡逆向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 加入过量Na2CO3溶液:Na+、Ca2+、NH4+、NO3-、H+ | |
| B. | 加入适量NaHCO3溶液:Na+、Ca2+、NH4+、NO3-、HCO3- | |
| C. | 加入适量NaOH溶液:Na+、Ca2+、NH4+、NO3-、OH- | |
| D. | 加入过量FeSO4和稀硫酸:Fe2+、Fe3+、NH4+、Ca2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
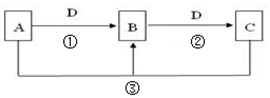 常见无机物A、B、C、D存在如图转化关系:
常见无机物A、B、C、D存在如图转化关系:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.82g青蒿素含氧原子数目为0.05NA | |
| B. | 标准状况下,1 mol青蒿素的体积为22.4 L | |
| C. | 青蒿素含氧量为10% | |
| D. | 青蒿素的摩尔质量为282 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com