
| A、使苯酚显紫色的溶液:NH4+、K+、SCN-、NO3- |
| B、加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- |
| C、c(C6H5OH)=0.1mol?L-1的溶液中:K+、HCO3-、SO42-、CO32- |
| D、由水电离产生的c(H+)=10-13mol?L-1的溶液:Fe2+、Na+、NO3-、SO42- |


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
| A、铁和硫酸铜溶液反应:Fe+Cu2+═Cu+Fe2+ |
| B、氢氧化铜与硫酸溶液反应:OH-+H+═H2O |
| C、碳酸钙与盐酸溶液反应:CO32-+2H+═H2O+CO2↑ |
| D、铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
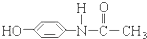 它可能具有的化学性质是( )
它可能具有的化学性质是( )| A、不与烧碱溶液反应 |
| B、能与溴水发生取代反应 |
| C、不能被氧化 |
| D、遇FeCl3溶液发生显色反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CH3CH2CH2OH |
| B、(CH3) 2CHCH(CH3) OH |
| C、(CH3) 3COH |
| D、(CH3) 2CHOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚丙烯的分子长链是由C-C键连接而成的 |
| B、聚丙烯分子的长链上有支链 |
| C、聚丙烯每个链节内含3个碳原子 |
| D、聚丙烯能使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H<0且熵增大的反应一定可以自发进行 |
| B、△H>0且熵减小的反应一定不能自发进行 |
| C、△H>0且熵增大的反应一定可以自发进行 |
| D、△H<0且熵减小的反应有可能可以自发进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com