
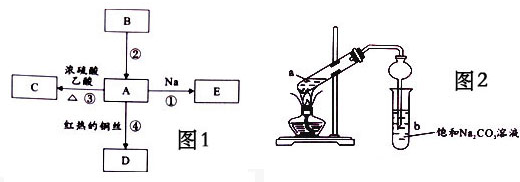
分析 B的产量可衡量一个国家石油化工发展的水平,B是乙烯,A是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,A能与Na、乙酸反应,在红热铜丝发生催化氧化,可推知A是乙醇,根据框图中的转化关系、反应条件和反应试剂可推得,C是乙酸乙酯,D是乙醛,E是乙醇钠,据此解答.
解答 解:B的产量可衡量一个国家石油化工发展的水平,B是乙烯,A是化学实验室中常见的有机物,它易溶于水并有特殊香味,根据框图中信息,A能与Na、乙酸反应,在红热铜丝发生催化氧化,可推知A是乙醇,根据框图中的转化关系、反应条件和反应试剂可推得,C是乙酸乙酯,D是乙醛,E是乙醇钠,
Ⅰ(1)根据上面的分析可知,B是乙烯,
故答案为:乙烯;
(2)反应②是乙烯与水发生加成反应得乙醇,
故答案为:加成反应;
(3)反应④是乙醇在铜作催化剂、加热条件下催化氧化生成乙醛,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
Ⅱ(4)在实验中球形干燥管除起冷凝作用外,另一个重要作用是防止液体倒吸,
故答案为:防止液体倒吸;
(5)试管b中观察到的现象是:液体分层,上层无色油状液体有果香味,
故答案为:液体分层,上层无色油状液体有果香味;
(6)8mL无水乙醇(ρ=0.79g/cm3)物质的量为$\frac{8×0.79}{46}$mol=0.14mol,6mL无水醋酸(ρ=1.05g/cm3)的物质的量为$\frac{6×1.05}{60}$mol=0.105mol,乙醇过量,所以生成的乙酸乙酯的物质的量为0.105mol,其质量为88×0.105g=9.24g,所以产率为$\frac{2.92}{9.24}$×100%=31.6%,
故答案为:31.6.
点评 考查有机推断、乙酸乙酯的制取,涉及烯、醇、羧酸的性质与转化等,难度不大,是对常见有机物知识的简单运用,注意掌握各类有机物的性质.


科目:高中化学 来源: 题型:选择题
| A. | 加入适量的6mol•L-1的盐酸 | B. | 加入数滴氯化铜溶液 | ||
| C. | 加入数滴硝酸铜溶液 | D. | 加入适量的氯化钠溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2有还原性,可被浓硫酸氧化 | |
| B. | NH3有还原性,可与浓硫酸发生氧化还原反应 | |
| C. | 在Cu和浓HNO3的反应中,参加反应的HNO3有$\frac{1}{2}$被还原 | |
| D. | 将胆矾加入浓H2SO4中,胆矾变白,这是浓硫酸的脱水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 转移溶液后未洗涤烧杯和玻璃棒就直接定容 | |
| B. | 称量时,在天平托盘上放上称量纸,将NaOH固体放在纸上称量 | |
| C. | 在容量瓶中进行定容时俯视刻度线 | |
| D. | 定容后把容量瓶倒置摇匀,发现液面低于刻度线,又补足了所缺的水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在标准状况下,1mol水的体积是22.4L | |
| B. | 在标准状况下,22.4L氦气所含的原子数约为2NA | |
| C. | 同温同压下,等体积的硫酸和硝酸所含氢原子数之比为2:1 | |
| D. | 1molCxHy分子中所含C-H数目为yNA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.21CCl4所含的分子数为0.5NA | |
| B. | 常温常压下,4.2gC2H4和C9H18混合物中含有的碳原子数为0.3NA | |
| C. | 7.8g苯分子中碳碳双键的数目为0.3NA | |
| D. | 常温下,1molC3H8含有C-H共价键数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)+△Q,0<△Q;使用和未使用催化剂时,反应过程中的能量变化 | |
| B. |  图②表示25℃时,用0.01mol•L-1盐酸滴定一定体积的0.01mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| C. |  图③表示CH4(g)+H2O(g)?CO(g)+3H2(g)+△Q,反应CH4的转化率与温度、压强的关系,且p1>p2、0<△Q | |
| D. |  图④中曲线表示反应2SO2(g)+O2(g)?2SO3(g)+△Q,0<△Q;正、逆反应的平衡常数K随温度的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下18g 铝放入足量浓硫酸中转移电子数2NA | |
| B. | 0.1mol•L-1的稀硫酸中含有H+个数为0.2NA | |
| C. | 常温常压下48g的O3中含有氧原子数为3NA | |
| D. | 1.8g NH4+中含有的电子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com