
 假设三: ;
假设三: ;
| | B装置的质量(g) | C装置的质量(g) | D装置的质量(g) |
| 实验前 | 15.4 | 262.1 | 223.8 |
| 试验后 | 6.1 | 264.8 | 230.4 |
 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 C
C 。
。| 实验次数 | 稀橙汁体积(mL) | 滴定用标准碘(水)溶液(mL) |
| 1 | 25.00 | 23.10 |
| 2 | 25.00 | 23.00 |
| 3 | 25.00 | 22.90 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+
溶液可以与酸性KMnO4溶液发生反应2MnO4-+5H2C2O4+6H+| 滴定次数 | 待测草酸溶液体积(mL) | 0.1000 mol/LKMnO4标准溶液体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 25.00 | 0.00 | 10.02 |
| 第二次 | 25.00 | 0.22 | 11.32 |
| 第三次 | 25.00 | 1.56 | 11.54 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
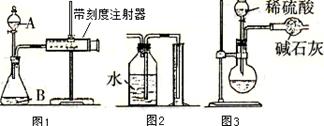
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 象是 ,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)
象是 ,说明反应放热。(下列装置中支撑及捆绑等仪器已略去)
 。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| | A | B | C | D |
| 纸蝴蝶上的喷洒液 | 石蕊 | 酚酞 | 酚酞 | 石蕊 |
| 小烧坏中的溶液 | 浓盐酸 | 浓氨水 | 氢氧化钠溶液 | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

 CO2无毒和无刺激性气味。
CO2无毒和无刺激性气味。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
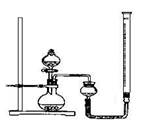
| 实验序号 | 双氧水体积 | 催化剂 | 待测数据 |
| a | 15mL | 无 | |
| b | 15mL | 0.5g CuO | |
| c | 15mL | 0.5g MnO2 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com