
| A. | K+、NH4+、OH-、SO42- | B. | H+、Fe2+、SO42-、ClO- | ||
| C. | Na+、Ca2+、Cl-、CO32- | D. | K+、Ca2+、Cl-、NO3- |
分析 A.铵根离子与氢氧根离子反应生成一水合氨;
B.亚铁离子、氢离子都与次氯酸根离子反应;
C.钙离子与碳酸根离子反应生成碳酸钙沉淀;
D.四种离子之间不发生反应,在溶液中能够共存.
解答 解:A.NH4+、OH-之间反应生成弱电解质一水合氨,在溶液中不能大量共存,故A错误;
B.H+、Fe2+都与ClO-发生反应,在溶液中不能大量共存,故B错误;
C.Ca2+、CO32-之间反应生成碳酸钙沉淀,在溶液中不能大量共存,故C错误;
D.K+、Ca2+、Cl-、NO3-之间不反应,在溶液中能够大量共存,故D正确;
故选D.
点评 本题考查离子共存,为高考的高频题,题目难度中等,注意掌握离子反应发生条件,明确离子之间不能共存的情况,如:发生复分解反应、发生氧化还原反应的离子等,试题培养了学生灵活应用基础知识的能力.


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案科目:高中化学 来源: 题型:解答题
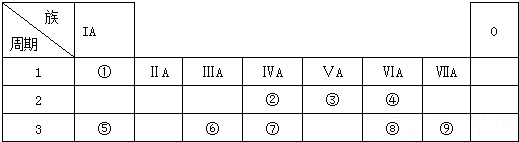
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表共有18个纵行 | |
| B. | 电子层数相同的原子一定属于同一周期 | |
| C. | 原子最外层电子数为2的元素一定在ⅡA族 | |
| D. | 62144Sm与62145Sm互为同位素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Z=18 | B. | X原子核内的中子数为20 | ||
| C. | Z=20 | D. | X原子核内的中子数为24 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 性质\元素 | 8O | 16S | 34Se | 52Te |
| 单质熔点(℃) | -218.4 | 113 | 450 | |
| 单质沸点(℃) | -183 | 444.6 | 685 | 1390 |
| 主要化合价 | -2 | -2,+4,+6 | -2,+4,+6 | |
| 原子半径 | 逐渐增大 | |||
| 单质与H2反应 | 点燃时易化合 | 加热化合 | 加热难化合 | 不能直接化合 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
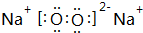 ,含有的化学键类型有离子键、共价键
,含有的化学键类型有离子键、共价键查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 此电池工作时会发出蓝色火焰 | |
| B. | 燃料电池具有能量转化率高、可持续使用的优点 | |
| C. | 该电池的负极电极反应式为:2H2+4e-═4H+ | |
| D. | 该电池的正极电极反应式为:O2+2H2O+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入BaCl2溶液有白色沉淀生成,加稀盐酸沉淀不消失,原溶液一定有SO42- | |
| B. | 加入AgNO3溶液有白色沉淀生成,加稀盐酸沉淀不消失,原溶液一定有Cl- | |
| C. | 加入盐酸产生能使澄清石灰水变浑浊的气体,原溶液中可能有CO32-或SO32- | |
| D. | 加入NaOH并加热,产生使湿润蓝色石蕊试纸变红的气体,原溶液是铵盐溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com