
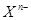 含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是
含中子N个,X的质量数为A,则ag X的氢化物中含质子的物质的量是 A.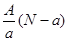 mol mol | B.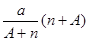 mol mol |
C.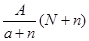 mol mol | D.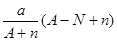 mol mol |
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源:不详 题型:单选题
| A.常温下11.2 L的甲烷气体含有甲烷分子数为0.5 NA个 |
| B.14g乙烯和丙烯的混合物中总原子数为3 NA个 |
| C.0.1 mol/L的氢氧化钠溶液中含钠离子数为0.1 NA个 |
| D.5.6 g铁与足量的稀硫酸反应失去电子数为0.3 NA个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.用少量水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡 |
| B.在盛有NaOH固体的烧杯中加入适量水溶解 |
| C.将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中 |
| D.将容量瓶盖紧,反复上下颠倒,摇匀 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1 L 1 mol?L-1的HAc溶液中含有氢离子数约为6.02×1023 |
| B.18 g D2O(重水)完全电解,转移的电子数约为6.02×1023 |
| C.标态下,22.4L NO2气体,所含氧原子数约为2×6.02×1023 |
| D.标态下,14g乙烯和丙烯的混合物中,含有共用电子对数目约为3×6.02×1023 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在常温常压下,16gO2和O3的混合气体所含原子数目为NA |
| B.1mol/LK2SO4溶液所含K+数目为2NA |
| C.在标准状况下,22.4L水所含分子数目为NA |
| D.7.8gNa2O2与CO2完全反应时,转移电子数目为0.2NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等物质的量的—CH3与—OH所含电子数相等 |
| B.7.80gNa2O2与5.85gNaC1所含阴离子数相等 |
| C.等质量的C2H4和C3H6中所含C—H键数相等 |
| D.等体积、等密度下的12C18O和14N2所含质子数相等 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.恒容加入l.5mol H2和0.5mol N2,充分反应后可得到NH3分子数为NA |
| B.一定条件下,2.3g的Na完全与O2反应生成3.6g产物时失去的电子数为0.1NA |
| C.常温常压下,22.4L Cl2与足量的铁粉反应,转移的电子数为2NA |
| D.标准状况下,22.4L的CH3CHO中含有的分子数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com