
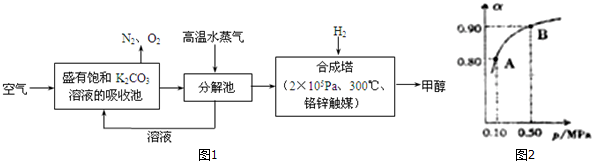
���� ��1�����ճ���ʢ�б���̼�����Һ�����տ����еĶ�����̼��ת��ΪKHCO3��̼����ز��ȶ����ڷֽ���м��ȷֽ�����̼��غͶ�����̼��ˮ��
��2��1mol������̼��Ӧ�ų�����Ϊ4947kJ��$\frac{1mol��44g/mol}{4400g}$=49.47kJ��ע�����ʵľۼ�״̬�뷴Ӧ����д�Ȼ�ѧ����ʽ��
��3������300����¶ȣ����Լӿ췴Ӧ���ʣ��Ҵ������Խϸߣ�
��4���ϳ����з�����Ӧ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g�������ɸ���ˮ���������ڷֽ����ѭ�����ã�
��5���ϳ����з�����Ӧ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����
��A�����ѹ������Ӧ���������Ũ�Ⱦ�����
B�����ѹ����ѹǿ���������淴Ӧ���ʶ�����
C��CO��H2��1��3�������Ͷ�룬�Ҷ��߰����ʵ���1��3��Ӧ����Ӧ��ϵ��CO2��H2�������ʼ��Ϊ1��3��
D��ѹ�����������ѹǿ��ƽ�������ƶ���CH3OH�������������
����ͼ��֪��0.1MPa������CO2��ƽ��ת����Ϊ0.8����֪��Ӧ��CO2Ϊ0.8mol�����ݷ���ʽ����μӷ�Ӧ�������ʵ������ٸ���v��������=$\frac{\frac{��n��������}{V}}{��t}$���㣻
��6��ԭ��ظ�������������Ӧ���״��ڸ���ʧȥ���ӣ���������������̼���������ˮ�������������ʵ���������OԪ�ػ��ϼ۱仯����ת�Ƶ��ӣ�
��� �⣺��1�����ճ���ʢ�б���̼�����Һ�����տ����еĶ�����̼��ת��ΪKHCO3��̼����ز��ȶ����ڷֽ���м��ȷֽ�����̼��غͶ�����̼��ˮ����Ӧ����ʽΪ��2KHCO3$\frac{\underline{\;\;��\;\;}}{\;}$K2CO3+H2O+CO2����
�ʴ�Ϊ��2KHCO3$\frac{\underline{\;\;��\;\;}}{\;}$K2CO3+H2O+CO2����
��2��1mol������̼��Ӧ�ų�����Ϊ4947kJ��$\frac{1mol��44g/mol}{4400g}$=49.47kJ���÷�Ӧ���Ȼ�ѧ����ʽΪ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.47KJ/mol��
�ʴ�Ϊ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����H=-49.47KJ/mol��
��3������300����¶ȣ����Լӿ췴Ӧ���ʣ��Ҵ������Խϸߣ�
�ʴ�Ϊ���ӿ췴Ӧ���ʣ�ʹ�������Խϸߣ�
��4���ϳ����з�����Ӧ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g�������ɸ���ˮ���������ڷֽ����ѭ�����ã�
�ʴ�Ϊ��H2O��
��5���ϳ����з�����Ӧ��CO2��g��+3H2��g��=CH3OH��g��+H2O��g����
��A�����ѹ������Ӧ���������Ũ�Ⱦ�����A����
B�����ѹ����ѹǿ���������淴Ӧ���ʶ�����B����
C��CO��H2��1��3�������Ͷ�룬�Ҷ��߰����ʵ���1��3��Ӧ����Ӧ��ϵ��CO2��H2�������ʼ��Ϊ1��3����C��ȷ��
D��ѹ�����������ѹǿ��ƽ�������ƶ���CH3OH�������������D��ȷ��
��ѡ��CD��
����ͼ��֪��0.1MPa������CO2��ƽ��ת����Ϊ0.8����֪��Ӧ��CO2Ϊ0.8mol�����ݷ���ʽ��֪�μӷ�Ӧ�������ʵ���Ϊ0.8mol��3=2.4mol����$\frac{\frac{2.4mol}{V}}{2min}$=1.2mol/��L��min�������V=1L��
�ʴ�Ϊ��1��
��6��ԭ��ظ�������������Ӧ���״��ڸ���ʧȥ���ӣ���������������̼���������ˮ�������缫��ӦΪ��CH3OH+8OH--6e-=CO32-+6H2O��
�������ʵ���Ϊ$\frac{6.72L}{22.4L/mol}$=0.3mol��ת�Ƶ���Ϊ0.3mol��4=1.2mol��
�ʴ�Ϊ��CH3OH+8OH--6e-=CO32-+6H2O��1.2��
���� ���⿼�黯ѧ��ҵ���̡��Ȼ�ѧ����ʽ��д����ѧƽ�������Ӱ�����ء��缫��Ӧʽ����д��֪ʶ�㣬�Ѷ��еȣ�ע��ȼ�ϵ���е缫��Ӧʽ����дҪ��ϵ������Һ������ԣ���Ȼȼ�Ϻ���������ͬ������������Һ��ͬ����缫��Ӧʽ�Ͳ�ͬ��


 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ѡ�� | ʵ��Ŀ�� | ʵ�鷽�� |
| A | ��֤��������Ư���� | ��������ͨ����ˮ�У�����Һ��ɫ�Ƿ���ɫ |
| B | �����Ȼ�����Һ���Ƿ�FeCl2 | ���Ȼ�����Һ�еμ�����������Һ |
| C | ����ʳ�����Ƿ�����KIO3 | ȡʳ������������KI��Һ�����������Һ���۲���Һ�Ƿ���� |
| D | ��֤Ksp��AgI����Ksp��AgCl�� | �����ʵ���NaCl��KI�Ļ��Һ�еμ�AgNO3��Һ���۲������ɫ |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
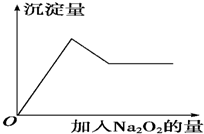 ��һ����Һ�����ܺ��нϴ�����Mg2+��Fe3+��Al3+��Cu2+��Na+��H+��SO42-��CO32-�е�һ�ֻ��֣�ȡ����Һ������ʵ��
��һ����Һ�����ܺ��нϴ�����Mg2+��Fe3+��Al3+��Cu2+��Na+��H+��SO42-��CO32-�е�һ�ֻ��֣�ȡ����Һ������ʵ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3H2S+2NO3-+2H+�T2NO��+3S��+4H2O | |
| B�� | 3Fe3++3NO3-+6H2S�T3NO��+6S��+3Fe2++6H2O | |
| C�� | Fe3++3NO3-+5H2S+2H+�T3NO��+5S��+Fe2++6H2O | |
| D�� | Fe3++9NO3-+14H2S+8H+�T9NO��+14S��+Fe2++18H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NaHSO3��NaHCO3�����Ի����Һ�У�S��C����R��ʾ����c��Na+��=c��HRO3-��+2c��RO32-�� | |
| B�� | �����½������ơ���������Һ��Ϻ���Һ�����ԣ����Ϻ���Һ�У�c��Na+����c��Cl-����c��CH3COOH�� | |
| C�� | ���������ʵ���Ũ����ȵĢ٣�NH4��2CO3���ڣ�NH4��2SO4���ۣ�NH4��2Fe��SO4��2������Һ��c��NH4+�����٣��ۣ��� | |
| D�� | ����������ʵ���Ũ�ȵ�NaClO��aq����NaCl��aq���������������٣�Nǰ��N�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʯͶ�뵽���������У�CO32-+2H+�TCO2��+H2O | |
| B�� | ����������������Һ�У�Fe+Fe3+�T2Fe2+ | |
| C�� | ��AlCl3��Һ�м�������İ�ˮ��Ӧ��Al3++3NH3•H2O�TAl��OH��3��+3NH4+ | |
| D�� | ��ϡ�����������������Һ�У�Ba2++SO42-�TBaSO4�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CuO�������� | B�� | Cu����ԭ�� | ||
| C�� | ͭ���������� | D�� | ͭԪ�ػ��ϼ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
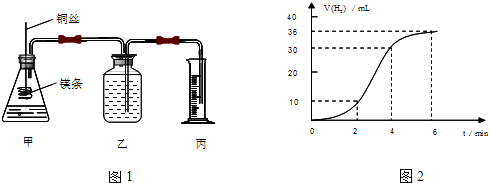
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | Mg��Al | B�� | Mg��Fe | C�� | Zn��Fe | D�� | Al��Zn |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com