
【题目】下列指定反应的离子方程式正确的是
A.Mg投入稀HNO3中:Mg+2H+=Mg2++H2↑
B.MnO2与浓盐酸混合加热制Cl2:MnO2+4H++4Cl-![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
C.向稀H2SO4和H2O2的混合液中加入Cu粉:2H++H2O2+Cu=Cu2++2H2O
D.向AlCl3溶液中加入过量氨水:Al3++4NH3·H2O=AlO![]() +2H2O+4NH
+2H2O+4NH![]()
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案科目:高中化学 来源: 题型:
【题目】![]() 是引起“温室效应”的主要物质,节能减排,高效利用化石能源,控制
是引起“温室效应”的主要物质,节能减排,高效利用化石能源,控制![]() 排放,探索
排放,探索![]() 的循环利用是保护环境,促进经济科持续发展的重要举措.
的循环利用是保护环境,促进经济科持续发展的重要举措.
(1)在一定温度下,向2L固定容积的密闭容器中通入2mol![]() ,3mol
,3mol![]() ,发生反应为:
,发生反应为:![]() ,测得
,测得![]() 和
和![]() 的浓度随时间变化如图1所示.
的浓度随时间变化如图1所示.
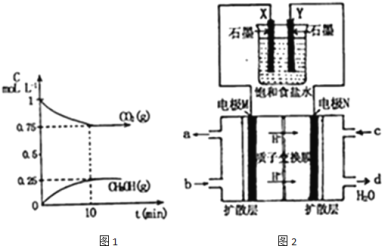
①能说明该反应已达到平衡状态的是 ______
A.![]() 体积分数在混合气体中保持不变
体积分数在混合气体中保持不变
B.单位时间内有![]()
![]() 断裂,同时有
断裂,同时有![]()
![]() 键生成
键生成
C.混合气体的密度不随时间变化
D.当体系中![]() :
:![]() :l,且保持不变
:l,且保持不变
②下列措施能使![]() 增大的是 ______
增大的是 ______
A.升高温度 ![]() 恒温恒容充入
恒温恒容充入![]()
![]() 使
使![]() 变成
变成![]()
D.恒温恒容下,再充入2mol![]() ,3mol
,3mol![]()
③计算该温度下此反应的平衡常数![]() ______ ;若使
______ ;若使![]() 应采取的措施是 ______
应采取的措施是 ______
A.增大压强![]() 恒压加入一定量
恒压加入一定量![]() C.恒容通入
C.恒容通入![]() D.降低温度
D.降低温度![]() 升高温度
升高温度
(2)如图2所示:用某甲醇燃料电池作电源电解饱和食盐水.
①写出电极N发生的反应式: ______
②若食盐水体积为300Ml,电解过程溶液体积变化忽略不计,常温下测得![]() 时,理论上消耗甲醇质量为 ______
时,理论上消耗甲醇质量为 ______ ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A. 标准状况下,5.6L 一氧化氮和5.6L 氧气混合后的分子总数为0.5NA
B. 等体积、浓度均为1mol/L的磷酸和盐酸,电离出的氢离子数之比为3:1
C. 一定温度下,1L 0.50 mol/L NH4Cl溶液与2L 0.25 mol/L NH4Cl溶液含NH4+的物质的量不同
D. 标准状况下,等体积的N2和CO所含的原子数均为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列各实验装置的叙述中,不正确的是( )
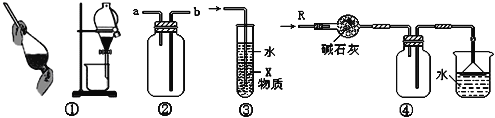
A. 装置②可用于收集H2、NH3、CO2、Cl2、HCl、NO2等气体
B. 装置③中X若为CCl4,可用于吸收NH3或HCl,并防止倒吸
C. 装置①可用于分离C2H5OH和H2O的混合物
D. 装置④可用于干燥、收集NH3,并吸收多余的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种化合物,均含有某种常见元素,它们的转化关系如下图所示,其中A为澄清溶液,C为难溶于水的白色固体,E则易溶于水,若取A溶液灼烧,焰色反应为浅紫色(透过蓝色钴玻璃)。请回答下列问题:

(1)写出化学式:A__________C__________
(2)写出下列反应的离子方程式:
A→B:________________________________。
B→D:________________________________。
C→E:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列六种物质:![]() 、
、![]() 、CaO、MgO、
、CaO、MgO、![]() 、
、![]() .
.
(1)按照不同的分类标准,它们中有一种物质与其他物质有明显的不同,请找出这种物质,并写出分类的依据.① ______②______.
(2)从反应中有无离子参加,可以将化学反应分为离子反应和非离子反应,![]() 与水反应的离子方程式是______.
与水反应的离子方程式是______.
(3)从上述氧化物中分别找出两种能相互反应的物质,写出一个非氧化还原反应的方程式和一个氧化还原反应的方程式,______.
(4)虽然分类的方法不同,但离子反应和氧化还原反应之间存在着一定的关系,请用简单的图示方法表示二者之间的关系:______.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向2L体积固定的密闭容器中加入1molHI,发生反应:2HIH2(g)+I2(g) H>0,测得![]() 的物质的量随时间变化如表,下列说法正确的是
的物质的量随时间变化如表,下列说法正确的是
| 1 | 2 | 3 |
|
|
|
|
A.2min内的HI的分解速度为![]()
![]()
B.该温度下,平衡时HI的转化率为1![]()
C.该温度下的平衡常数为![]() ,温度升高10℃后平衡常数为
,温度升高10℃后平衡常数为![]() ,则K1>K2
,则K1>K2
D.达平衡后其他条件不变,压缩容器体积,平衡不移动,![]() 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为![]() 时,在三个容积均为
时,在三个容积均为![]() 的恒容密闭容器中仅发生反应:
的恒容密闭容器中仅发生反应:![]() 正反应吸热
正反应吸热![]() 。实验测得:
。实验测得:![]() ,
,![]() ,
,![]() 、
、![]() 为速率常数,受温度影响。平衡常数
为速率常数,受温度影响。平衡常数![]() 是用平衡分压代替平衡浓度计算,分压
是用平衡分压代替平衡浓度计算,分压![]() 总压
总压![]() 物质的量分数。下列说法不正确的是
物质的量分数。下列说法不正确的是![]()
![]()
容器 编号 | 物质的起始浓度 | 物质的平衡浓度 | ||
|
|
|
| |
Ⅰ |
| 0 | 0 |
|
Ⅱ |
|
|
| |
Ⅲ | 0 |
|
| |
A.达平衡时,容器Ⅱ中![]() 比容器Ⅰ中的小
比容器Ⅰ中的小
B.容器Ⅱ反应达平衡前,![]()
C.起始时容器Ⅰ中总压强为![]() ,则
,则![]() 时该反应的平衡常数
时该反应的平衡常数![]() kPa
kPa
D.当温度改变为![]() 时,若
时,若![]() 则
则![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.1mol/L的CH3COOH溶液中存在如下电离平衡:CH3COOH![]() CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A.加入少量NaOH固体,平衡向正反应方向移动,溶液中c(H+)增大
B.加水,平衡向正反应方向移动,c(CH3COO-)和c(H+)增大
C.加入少量HCl,平衡逆向移动,溶液中c(H+)减少
D.加入少量CH3COONa固体,平衡向逆反应方向移动,溶液导电能力增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com