�-������ͭ��������Ļ���������Cu
4O��PO
4��
2����ͨ�����з�Ӧ�Ʊ���2Na
3PO
4+4CuSO
4+2NH
3?H
2O=Cu
4O��PO
4��
2��+3Na
2SO
4+��NH
4��2SO
4+H
2O��
��ش��������⣮
��1����������ʽ���漰����N��OԪ�ص縺����С�����˳����
��
��2����̬S�ļ۵����Ų�ʽΪ
����Cuͬ������������������ȵ�Ԫ�ػ���
����Ԫ�ط��ţ���
��3��PO
43-�Ŀռ乹���ǣ�����Pԭ�ӵ��ӻ���ʽΪ
��
��4��������ͭ��Һ�м��������KSCN��Һ�����������[Cu��CN��4]
2-��1molCN
-�к��еĦм�����ĿΪ
��
��5��ͭ����Ϊ�����������ܼ��ѻ���ͭ��ԭ�Ӱ뾶Ϊ127.8pm����ʽ���㾧��ͭ���ܶ�
g/cm
3��
��6���±��г��˺���������ǿ������ǻ���ԭ�����Ĺ�ϵ��
| ������ | ���� | ���� | ������ |
| ������ | Cl-OH | 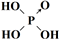 | 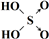 |  |
| ���ǻ���ԭ���� | 0 | 1 | 2 | 3 |
| ���� | ���� | ��ǿ�� | ǿ�� | ��ǿ�� |
�ɴ˿ɵó����жϺ�����ǿ����һ�����������
�������ᣨH
3PO
3��Ҳ����ǿ�ᣬ���ĽṹʽΪ
�������������������������Һ��Ӧ�Ļ�ѧ����ʽΪ
��

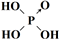
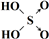

 �����������ǻ��е����ܱ����������кͣ�����1molH3PO3����2molNaOH��Ӧ����Ӧ�Ļ�ѧ����ʽΪH3PO3+2NaOH=Na2HPO3+2H2O��
�����������ǻ��е����ܱ����������кͣ�����1molH3PO3����2molNaOH��Ӧ����Ӧ�Ļ�ѧ����ʽΪH3PO3+2NaOH=Na2HPO3+2H2O�� ��H3PO3+2NaOH=Na2HPO3+2H2O��
��H3PO3+2NaOH=Na2HPO3+2H2O��


 �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�