
| �������� | Fe��OH��3 | Al��OH��3 | Mg��OH��2 |
| ��ʼ����pH | 1.5 | 3.3 | 9.4 |
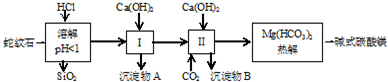
���� ����ʯ����Կ�����MgO��Fe2O3��Al2O3��SiO2��ɣ����ܹ��˵õ���Һ��ΪMg2+��Fe3+��Al3+�������������Ƴ����õ�����������������������A����Һ��ͨ�������̼����������������B��̼����ƣ������������Ʒ�Ӧ����̼���ѭ�����ã���Һ�еõ�̼����þ��Һ���Ƚ�õ���ʽ̼��þ��
��1������ʯ����Կ���MgO��Fe2O3��Al2O3��SiO2��ɣ�����ʯ�������ܽ��MgO��Fe2O3��Al2O3��HCl��Ӧ�ܽ⣬��SiO2��HCl����Ӧ�������ܽ⣻
��2�����������ƹ���ʱ����Һ������ǿ��Al��OH��3���ܽ⣬���������������pH���пɿ�����Mg��OH��2��pHΪ9.4ʱ��ʼ���������Լ�����ǿMg��OH��2�������
��3����ɫ������ΪFe2O3��Ӧ�Ƚ����к��е�����Al��OH��3��ȥ����ȥAl��OH��3�ķ�����������������ǿ������ʣ�
��4��̼����þ�ȷֽ����ɼ�ʽ̼��þ��������̼��ˮ������ͬ������̼��þ�ͼ�ʽ̼��þ��þ�����ʵ������ߴ������
��5���˹�����CO2�ǿ����ظ�ʹ�õģ�
��6�����������ӳ�����ȫ��PH����������þ��������þ��̼��þ�����ᷴӦ��������PH���������ӣ���ȥMgCl2������Һ�е�Fe3+��
��� �⣺����ʯ����Կ�����MgO��Fe2O3��Al2O3��SiO2��ɣ����ܹ��˵õ���Һ��ΪMg2+��Fe3+��Al3+�������������Ƴ����õ�����������������������A����Һ��ͨ�������̼����������������B��̼����ƣ������������Ʒ�Ӧ����̼���ѭ�����ã���Һ�еõ�̼����þ��Һ���Ƚ�õ���ʽ̼��þ��
��1������ʯ�������ܽ⣬MgO��Fe2O3��Al2O3��HCl��Ӧ�ܽ⣬��Ӧ����ʽ�ֱ�Ϊ��MgO+2HCl=MgCl2+H2O��Fe2O3+6HCl=2FeCl3+3H2O��Al2O3+6HCl=2AlCl3+3H2O����SiO2�������ᷴӦ���Գ�������ʽ��ȥ��
�ʴ�Ϊ��Fe3+��Al3+��
��2���ɣ�1��֪����ʱ��Һ�г���Mg2+�⣬������Fe3+��Al3+���ʣ����ȥFe3+��Al3+��������ʧMg2+����Fe3++3H2O?Fe��OH��3+3H+��Al3++3H2O?Al��OH��3+3H+������ƽ���ƶ���ԭ��������H+ʹ����ˮ��ƽ��������Ӧ�����ƶ�����ȥFe3+��Al3+����Ca��OH��2�轫��Һ��pH������7��8����pH���ߣ��ᵼ�����ɵ�Al��OH��3������ӦAl��OH��3+OH-=AlO2-+2H2O�ܽ⣬Mg��OH��2��pHΪ9.4ʱ��ʼ���������Լ�����ǿMg��OH��2�������ͬʱMg2+Ҳ��ת��Ϊ��������ʧ��
�ʴ�Ϊ��Al��OH��3��Mg��OH��2��
��3����ʵ�鲽��ͼ֪�����������ΪFe��OH��3��Al��OH��3����ɫ�������dz�����Fe��OH��3�ֽ��õ���Fe2O3�����Ե��ȼӼ��Al��OH��3��������ӦΪ��Al��OH��3+NaOH=NaAlO2+2H2O��Ȼ�����ϴ�����ռ��ɣ�
�ʴ�Ϊ��NaOH��ϴ�ӡ����գ�
��4��̼����þ�ȷֽ����ɼ�ʽ̼��þ��������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��2 Mg��HCO3��2$\frac{\underline{\;\;��\;\;}}{\;}$Mg2��OH��2CO3+3CO2��+H2O�����ȷֽⲻ��ȫ�����ü�ʽ̼��þ�н�����MgCO3��ͬ������̼��þ�ͼ�ʽ̼��þ��þ�����ʵ�����̼��þ��þԪ�����ʵ���$\frac{1}{84}$����ʽ̼��þ��þԪ�����ʵ���$\frac{1}{142}��2$=$\frac{1}{71}$����ʽ̼��þ�к�þ�����ȷֽⲻ��ȫ�����ü�ʽ̼��þ�н�����MgCO3����Ʒ��þ������С�����Ʒ��þ�������������ͣ�
�ʴ�Ϊ��2 Mg��HCO3��2$\frac{\underline{\;\;��\;\;}}{\;}$Mg2��OH��2CO3+3CO2��+H2O�����ͣ�
��5����ʵ�鲽��ͼ֪������ʵ���У��������ͨ������̼������̼��ƣ�̼��Ʒֽ�ɵõ�������̼����Ϊ�ڢ�ԭ�ϣ���ʽ̼��þ�ֽ�õ�CO2������ѭ��ʹ�õ�������CO2��
�ʴ�Ϊ��CO2��
��6����������þ��������þ��̼��þ�����ᷴӦ��������PH���������ӣ���ȥMgCl2������Һ�е�Fe3+����ȥMgCl2������Һ�е�Fe3+�����ڼ��ȡ�����������¼���MgO��Mg��OH��2��MgCO3 ���˺��ټ����������ᣬ
�ʴ�Ϊ��MgO��Mg��OH��2��MgCO3��
���� ������Ҫ������Ԫ�ػ������н��������������ʣ�����ʱ��������֪���ʼ�ķ�Ӧԭ�����������������ʵ�����ƣ��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����������ϡ�����У�FeS+2H+=Fe2++H2S�� | |
| B�� | ������NaOH��Һ����NH4HCO3��Һ�У�HCO3-+OH-=CO32-+H2O | |
| C�� | ����SO2ͨ�뱽������Һ�У�C6H5O-+SO2+H2O=C6H5OH+HSO3- | |
| D�� | ����ʯ���ڴ����У�CaCO3+2H+=Ca2++CO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �������еμӰ�ˮ��H++OH-�TH2O | |
| B�� | Fe��OH��3��������Fe��OH��3+3H+�TFe3++3H2O | |
| C�� | ͭ����ϡ���3Cu+8H++2NO3-�T3Cu2++2NO��+4H2O | |
| D�� | ����������Һ��ͨ�����CO2��Ca2++2ClO-+H2O+CO2�TCaCO3��+2HClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ����� | ʵ�� | ʵ������ | ���� |
| ʵ��� | ��ʵ������ռ����������ȼ | ����ȼ�գ�����ʵ���ɫ | ����ɷ�Ϊ���� |
| ʵ��� | ��ʵ����еİ�ɫ�������˳���ϴ�ӣ�ȡ������������ϡ���� | �������ݳ���ȫ���ܽ� | ��ɫ�������к���MgCO3 |
| ʵ��� | ȡʵ����е���Һ�������м�������CaCl2��BaCl2ϡ��Һ | ������ɫ��������Һ��ɫ��dz | ��Һ�д���CO${\;}_{3}^{2-}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | MgCl2  | B�� | CCl4  | C�� | CO2  | D�� | Na2O  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | FeS2$\stackrel{����}{��}$SO3$\stackrel{H_{2}O}{��}$H2SO4 | |
| B�� | NaCl��aq��$\stackrel{���}{��}$Na$\stackrel{O_{2}}{��}$Na2O2 | |
| C�� | Fe$\stackrel{ϡH_{2}SO_{4}}{��}$FeSO4��aq��$\stackrel{NaOH��aq��}{��}$Fe��OH��2$\stackrel{����������}{��}$Fe2O3 | |
| D�� | Fe2O3$\stackrel{����}{��}$FeCl3��aq��$\stackrel{Cu}{��}$Fe |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com