
| A、该反应达到平衡时,放出的热量等于92.4kJ |
| B、达到平衡后向容器中通入1mol氦气,平衡正向移动 |
| C、若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的80% |
| D、若达到平衡时N2的转化率为20%,则平衡时容器内的压强是起始时的90% |
| 4-0.4 |
| 4 |
| 4-0.4 |
| 4 |


 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
| A、①②⑥ | B、③④⑥ |
| C、③⑤⑥ | D、③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
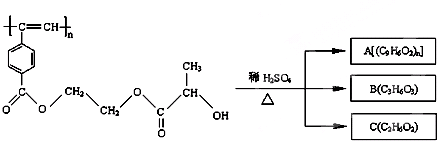
| A、M、A均能使酸性高锰酸钾溶液和溴水褪色 |
| B、B中含有羧基和羟基两种官能团,B能发生消去反应和酯化反应 |
| C、1molM与热的烧碱溶液反应,可消耗2n mol的NaOH |
| D、A、B、C各1mol分别与金属钠反应,放出的气体的物质的量之比为1:2:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、放电时负极:Cd-2e-=Cd2+ |
| B、充电时阳极:Cd(OH)2+2e-=Cd+2OH- |
| C、充电时阳极:2Ni(OH)2-2e-+4H+=2Ni3++4H2O |
| D、放电时正极:2NiOOH+2e-+2H2O=2Ni(OH)2+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学反应速率可表示可逆反应进行的程度 |
| B、根据化学反应速率的大小可知化学反应进行的快慢 |
| C、化学反应速率是指一定时间内,任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
| D、对于任何化学反应来说,反应速率越大,反应现象越明显 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1NaHS溶液:c(OH-)+c(S2-)=c(H2S )+c(H+) |
| B、0.1 mol?L-1NaHCO3溶液:c(Na+)>c(HCO3-)>c(OH-)>c(CO32-)>c(H+) |
| C、Na2CO3溶液:c(OH-)=c(H+)+c(HCO3-)+2c(H2CO3) |
| D、0.1 mol?L-1氨水:c(NH4+)+c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2 |
| B、N2O |
| C、NO |
| D、NO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能电离出H+的化合物就是酸 |
| B、在水溶液里或熔融状态下能导电的物质是电解质 |
| C、离子方程式Cu2++2OH-=Cu(OH)2↓只能表示一个化学反应 |
| D、溶液、胶体和浊液最本质的区别是分散质粒子的大小不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18和12 | B、6和8 |
| C、12和16 | D、12和17 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com