


分析 饱和一元醇A中氧的质量分数约为21.6%,设该一元醇的通式为CnH2n+2O,氧元素的质量分数=$\frac{16}{16+14n+2}$=21.6%,n=4,则A的分子式为C4H10O,结构分析显示A只有一个甲基,则A的结构简式为CH3CH2CH2CH2OH,A在Cu作催化剂、加热条件下被氧化生成B,B能发生银镜反应,则B结构简式为CH3CH2CH2CHO,1-丁醛在NaOH/H2O条件下发生加成生成C,C结构简式为CH3CH2CH2CH=C(CH2CH3)CHO,C反应生成D,E为水杨酸酯,根据图中转化关系知,D中含有醇羟基,且D相对分子质量为130,则D结构简式为CH3CH2CH2CH2CH(CH2CH3)CH2OH,C和氢气发生加成反应生成D,D和邻羟基苯甲酸发生酯化反应生成E,E结构简式为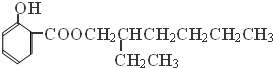 ,据此分析解答.
,据此分析解答.
解答 解:饱和一元醇A中氧的质量分数约为21.6%,设该一元醇的通式为CnH2n+2O,氧元素的质量分数=$\frac{16}{16+14n+2}$=21.6%,n=4,则A的分子式为C4H10O,结构分析显示A只有一个甲基,则A的结构简式为CH3CH2CH2CH2OH,A在Cu作催化剂、加热条件下被氧化生成B,B能发生银镜反应,则B结构简式为CH3CH2CH2CHO,1-丁醛在NaOH/H2O条件下发生加成生成C,C结构简式为CH3CH2CH2CH=C(CH2CH3)CHO,C反应生成D,E为水杨酸酯,根据图中转化关系知,D中含有醇羟基,且D相对分子质量为130,则D结构简式为CH3CH2CH2CH2CH(CH2CH3)CH2OH,C和氢气发生加成反应生成D,D和邻羟基苯甲酸发生酯化反应生成E,E结构简式为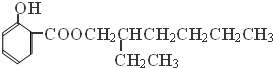 ,
,
(1)通过以上分析知,A的分子式为C4H10O,A的名称为1-丁醇,
故答案为:C4H10O;1-丁醇;
(2)B结构简式为CH3CH2CH2CHO,B和银氨溶液发生银镜反应,该反应的化学方程式为CH3CH2CH2CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$ CH3CH2CH2COONH4+2Ag↓+3NH3+H2O,
故答案为:CH3CH2CH2CHO+2[Ag(NH3)2]OH$\stackrel{△}{→}$ CH3CH2CH2COONH4+2Ag↓+3NH3+H2O;
(3)C中含有醛基和碳碳双键,都能和溴水反应,要检验两种官能团,则应先用银氨溶液检验醛基,然后再用溴水检验碳碳双键,所以所加试剂先后顺序是:银氨溶液、稀盐酸、溴水,
故答案为:银氨溶液、稀盐酸、溴水;
(4)A~D中是A和D都是一元醇,互为同系物,D为CH3CH2CH2CH2CH(CH2CH3)CH2OH,属于醇,E为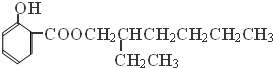 ,有酚羟基,可以用FeCl3溶液或浓溴水加以区别,
,有酚羟基,可以用FeCl3溶液或浓溴水加以区别,
故答案为:有;FeCl3溶液或浓溴水.
点评 本题考查有机物推断,侧重考查分析、推断能力,难度中等,正确推断A结构是解本题关键,注意题给信息中两个醛分子反应时断键和成键方式.


科目:高中化学 来源: 题型:选择题
 如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图;装置(Ⅰ)的离子交换膜只允许Na+通过.已知电池充、放电的化学方程式为2Na2S2+NaBr3 $?_{充电}^{放电}$Na2S4+3NaBr.当闭合开关K时,X极附近溶液先变红色.下列说法中正确的是( )
如图所示,装置(Ⅰ)是一种可充电电池的示意图,装置(Ⅱ)为电解池的示意图;装置(Ⅰ)的离子交换膜只允许Na+通过.已知电池充、放电的化学方程式为2Na2S2+NaBr3 $?_{充电}^{放电}$Na2S4+3NaBr.当闭合开关K时,X极附近溶液先变红色.下列说法中正确的是( )| A. | 闭合K时,装置(Ⅰ)中Na+从右到左通过离子交换膜 | |
| B. | 闭合K时,A电极的电极反应式为NaBr3+2Na++2e-═3NaBr | |
| C. | 闭合K时,X电极的电极反应式为2Cl--2e-═Cl2↑ | |
| D. | 闭合K时,当有0.1 mol Na+通过离子交换膜,则X电极上析出气体在标准状况下的体积为1.12 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Ba(OH)2溶液中加入过量的NaHCO3溶液:HCO3-+Ba2-+OH-═BaCO3↓+H2O | |
| B. | 向小苏打溶液中加入过量石灰水,Ca2++2OH-+2HCO3-=CaCO3↓+CO32-+2H2O | |
| C. | 向硫酸氢钠溶液中加入过量氢氧化钡溶液:2HSO4-+2Ba2++2OH-=2BaSO4↓+2H2O | |
| D. | 向碳酸氢钙溶液中加入过量石灰水:Ca2++HCO3-+OH-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 煤的气化是物理变化 | |
| B. | 石油裂解的主要目的是为了得到更多的汽油 | |
| C. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| D. | 煤干馏得到的煤焦油中有芳香烃 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚与碳酸氢钠溶液反应:C6H5OH+HCO3-→C6H5O-+CO2↑+H2O | |
| B. | 溴乙烷转化成乙醇:C2H5Br+OH- $→_{△}^{水}$C2H5OH+Br- | |
| C. | 肥皂液加入醋酸:C17H35COO-+H+→C17H35COOH | |
| D. | 甲醛溶液与足量的新制Cu(OH)2共热:HCHO+2Cu(OH)2+OH-$\stackrel{△}{→}$HCOO-+Cu2O↓+3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:
氨气是一种富氢燃料,可以直接用于燃料电池,如图是供氨水式燃料电池工作原理:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 己二酸二乙酯是乙酸纤维素、硝酸纤维素的增塑剂,实验室合成己二酸二乙酯的反应原理和有关数据如下:
己二酸二乙酯是乙酸纤维素、硝酸纤维素的增塑剂,实验室合成己二酸二乙酯的反应原理和有关数据如下: +2C2H5OH$?_{甲苯/△}^{浓硫酸}$
+2C2H5OH$?_{甲苯/△}^{浓硫酸}$ +2H2O
+2H2O| 相对分子质量 | 密度/(g•cm-3) | 沸点/℃ | 水中溶解性 | |
| 己二酸二乙酯 | 202 | 1.01 | 245 | 不溶于水 |
| 己二酸 | 146 | 1.36 | 231.8 | 微溶 |
| 乙醇 | 46 | 0.79 | 78.4 | 混溶 |
| 甲苯 | 92 | 0.87 | 110.6 | 不溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在水溶液中,HCO3-仅仅发生水解 | |
| B. | 在水溶液中,HCO3-仅仅发生电离 | |
| C. | 在水溶液中,HCO3-的水解程度要大于电离程度 | |
| D. | 在水溶液中,HCO3-的电离程度要大于水解程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图装置中,U型管内为红墨水,a,b试管内分别盛有是食盐水和醋酸溶液,各加入生铁快,放置右方时间,请回答下列问题:
如图装置中,U型管内为红墨水,a,b试管内分别盛有是食盐水和醋酸溶液,各加入生铁快,放置右方时间,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com