
一定条件下氨气和氧化铜可以发生如下反应:2NH3+3CuO 3Cu+N2+3H2O,下列对此反应的分析中合理的是()
3Cu+N2+3H2O,下列对此反应的分析中合理的是()
A. 该反应属于置换反应
B. CuO是氧化剂
C. 反应体现了金属铜的还原性
D. 每生成1molH2O就伴随着1mol电子转移
考点: 氧化还原反应.
分析: A.单质与化合物反应生成单质与化合物,为置换反应;
B.Cu元素的化合价降低;
C.Cu为生成物;
D.由反应可知,生成3molH2O,转移6mol电子.
解答: 解:A.单质与化合物反应生成单质与化合物,为置换反应,该反应的反应物中没有单质,不属于置换反应,故A错误;
B.Cu元素的化合价降低,则CuO为氧化剂,故B正确;
C.Cu为生成物,该反应中CuO为氧化剂,氨气为还原剂,具有还原性,故C错误;
D.由反应可知,生成3molH2O,转移6mol电子,则每生成1molH2O就伴随着2mol电子转移,故D错误;
故选B.
点评: 本题考查氧化还原反应,为2015届高考高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应中基本概念及置换反应判断的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
某主族元素R的最高化合价与负化合价代数和为6.下列说法正确的是()
A. R的气态氢化物能燃烧
B. R的最高价氧化物为RO3
C. R一定是第ⅦA族元素
D. R的气态氢化物易溶于水显碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
当下列各组物质的总物质的量不变时,使各组分以任意比混合后充分燃烧,消耗氧气的量和生成CO2的物质的量不变的是( )
|
| A. | 乙烯、乙醇、乙醛 | B. | 乙炔、乙醛、乙二醇 |
|
| C. | 甲烷、甲醇、乙酸 | D. | 甲烷、甲酸甲酯、丙二酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法错误的是()
A. 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性
B. 等物质的量浓度的醋酸与醋酸钠溶液中水电离产生的c(OH﹣).前者小于后者
C. 沉淀溶解达到平衡时,溶液中溶质的离子浓度不一定相等,但保持不变
D. 水的离子积只与温度有关,向水中加入酸、碱或盐一定会影响水的电离平衡
查看答案和解析>>
科目:高中化学 来源: 题型:
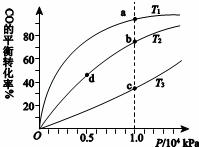
用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)⇌CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与 压强的关系如右下图所示.下列说法正确的是()
压强的关系如右下图所示.下列说法正确的是()
A.温度: T1>T2>T3
B.正反应速率: υ(b)>υ(d) υ(a)>υ(c)
C.平衡常数: K(a)>K(c) K(b)=K(d)
D.平均摩尔质量: M(b)>M(d) M(a)<M(c)
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
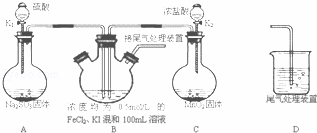
某化学实验小组为验证常见还原剂SO2、I﹣、Fe2+的还原性强弱的顺序为:SO2>I﹣>Fe2+,用图所示装置进行实验(加热和夹持装置已略,气密性已检验).
(1)上述实验需要加热的装置是
(2)A中反应的化学方程式为
(3)D中,烧杯盛放的是
(4)实验开始时,关闭K1,打开K2,通入少量氯气,写出B中发生反应的离子方程式
①为验证I﹣的还原性比Fe2+强,取(4)后B中的少量溶液于试管中,应再往试管中滴入 溶液,现象是
②在(4)后,为了比较SO2和I﹣的还原 性强弱,接下来的操作是
性强弱,接下来的操作是
A.打开K1 B.打开K2 C.同时打开K1和K2
(5)若打开K2,通入Cl2恰好将Fe2+、I﹣全部氧化后,再打开K1通入SO2,当Fe3+全部转化为Fe2+时,此时通入的SO2的体积(标准状况下)为 L
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的值,下列有关叙述不正确的是()
A. 26g C2H2和苯蒸气的混合气体中所含的C原子数为2NA
B. 1mol甲基(﹣CH3)所含电子数为9NA
C. 标准状况下,B2H6和C2H4的混合气体22.4L,所含的电子数约为16NA
D. 标准状况下,1L庚烷所含有的分子数为NA/22.4
查看答案和解析>>
科目:高中化学 来源: 题型:
0.2mol有机物和0.4mol O2在密闭容器中燃烧后的产物为CO2、CO和H20(气),产物通过浓硫酸,浓硫酸质量增加10.8g;再通过灼热CuO,充分反应后,CuO质量减轻3.2g;最后气体再通过碱石灰被完全吸收,碱石灰质量增加17.6g.
(1)试推断该有机物的分子式.
(2)若0.2mol该有机物恰好与9.2g金属钠完全反应,试确定该有机物的结构简式并命名.
查看答案和解析>>
科目:高中化学 来源: 题型:
近年来,为满足某些尖端技术的发展需要,人们又设计和合成了许多新型合金材料。如:储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料。此外,________、________和________等新型合金广泛应用于卫星、航空航天、生物工程和电子工业等领域。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com