
| 反应时间 | CO2(mol) | H2(mol) | CH3OH(mol) | H2O(mol) | |
| 反应Ⅰ 恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 反应Ⅱ 绝热恒容 | 0min | 0 | 0 | 2 | 2 |
分析 Ⅰ、依据热化学方程式和盖斯定律计算所得热化学方程式;
Ⅱ、(1)①自发进行的判断依据是△H-T△S<0,结合反应特征分析判断需要的条件;
②平衡标志是正逆反应速率相同,个组分含量保持不变,原则是变量不变分析选项;
③图象t2起点,t3 到t4终点,t4以后符合变化趋势即可,在t2时将容器容积缩小一倍,压强增大,二氧化碳浓度增大,平衡正向进行,随后减小,t3时达到平衡,t4时降低温度,平衡正向进行,二氧化碳减小,反应速率减小,t5时达到平衡;
(2)①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,反应Ⅰ是恒温恒容容器,Ⅱ为恒容绝热,反应是放热反应,图表中反应ⅠⅡ若恒温恒容达到相同平衡状态,Ⅱ为逆向恒容绝热,温度降低,平衡正向进行,平衡常数增大,甲醇浓度增大;
②反应速率V=$\frac{△c}{△t}$计算得到氢气反应速率,速率之比等于化学方程式计量数之比计算甲醇反应速率;依据平衡三段式列式计算分析平衡状态的物质的量.
解答 解:Ⅰ. 已知:H2的热值为142.9KJ•g-1 ,燃烧热为285.8KJ/mol,
①H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8KJ/mol
②N2(g)+2O2(g)=2NO2(g)△H=+133kJ•mol-1
③H2O(g)=H2O(l)△H=-44kJ•mol-1
①×4-②-③×4得到催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1;
故答案为:4H2(g)+2NO2(g)=N2(g)+4H2O(g)△H=-1100.2kJ•mol-1;
Ⅱ.(1)①CO2(g)+3H2(g)═CH3OH(l)+H2O(l),熵变△S<0,则反应焓变△H<0,低温下满足△H-T△S<0
故答案为:低温;
②CO2(g)+3H2(g)═CH3OH(l)+H2O(l),
a、混合气体的平均式量始终保持不变,不能说明反应达到平衡状态,故a错误;
b、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,所以过程中CO2和H2的体积分数始终保持不变,故b错误;
c、向2L密闭容器中加入2mol CO2、6mol H2,按照1:3反应,CO2和H2的转化率始终相等,不能确定反应是否达到平衡状态,故c错误;
d、反应物是气体,生成物是液体,混合气体的密度保持不变,说明反应达到平衡状态,故d正确;
e、1mol CO2生成的同时有3mol H-H键断裂,说明正逆反应速率相同,反应达到平衡状态,故e正确;
故答案为:d e;
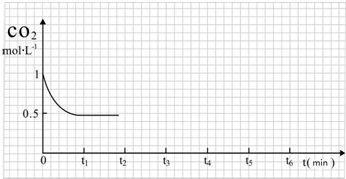
③在t2时将容器容积缩小一倍,压强增大,二氧化碳浓度增大,平衡正向进行,随后减小,t3时达到平衡,t4时降低温度,平衡正向进行,二氧化碳减小,反应速率减小,t5时达到平衡;
图象t2起点二氧化碳浓度突然增大为1mol/L,随反应进行减小,图中t3 到t4终点平衡线在0.5的线上,t4t4以后在0.5线以下,但不能到横坐标线上且有平衡线段,图象为: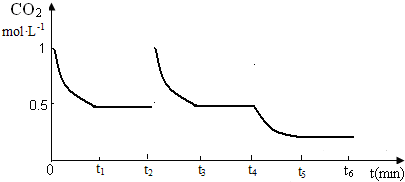 ;
;
故答案为:
(2)①CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H<0,反应Ⅰ是恒温恒容容器,Ⅱ为恒容绝热,反应是放热反应,图表中反应ⅠⅡ若恒温恒容达到相同平衡状态,Ⅱ为逆向恒容绝热,温度降低,平衡正向进行,平衡常数增大,甲醇浓度增大;
故答案为:<;<;
②CO2(g)+3H2(g)═CH3OH(g)+H2O(g)
起始量(mol) 2 6 0 0
变化量(mol) 1 3 1 1
30min量(mol) 1 3 1 1
对反应I,前10min内的平均反应速率v(CH3OH)=$\frac{1}{3}$v(H2)=$\frac{1}{3}$×(6-4.5)mol2L10min=0.025mol•L-1•min-1;
若30min时只改变温度为T2℃,此时H2的物质的量为3.2mol,氢气增加,说明平衡逆向进行,温度升高T2>T1,若30min时只向容器中再充入1mol CO2(g)和1mol H2O(g),对正逆反应的影响程度相同,平衡不变;
故答案为:0.025mol•L-1•min-1 ;<;不.
点评 本题考查了热化学方程式书写,平衡影响因素分析判断,平衡计算的分析应用,注意恒温恒容和恒容绝热容器的分析判断,掌握基础是关键,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
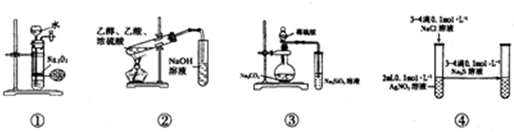
| A. | 装置①可制备少量氧气 | |
| B. | 装置②可用于实验室制取和收集乙酸乙酯 | |
| C. | 装置③的实验可推断硫、碳、硅三种元素的非金属强弱 | |
| D. | 装置④能验证AgCl沉淀可转化为溶解度更小的Ag2S沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用饱和食盐水替代水与电石反应,可以减缓乙炔的产生速率 | |
| B. | 配制一定物质的量浓度的溶液定容时,俯视刻度线会使浓度偏低 | |
| C. | 测定中和反应的反应热时,将碱缓慢倒入酸中,不影响测定结果 | |
| D. | 用NaOH标准液滴定待测浓度盐酸,达终点时滴定管尖嘴有悬滴,则测定结果偏小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 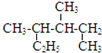 的系统命名是2,3-二甲基戊烷 的系统命名是2,3-二甲基戊烷 | |
| B. | 向鸡蛋清溶液中分别加入(NH4)2SO4和CuSO4溶液都能使鸡蛋清聚沉,其作用原理相同 | |
| C. | 丙烯酸(CH2=CHCOOH)和山梨酸(CH3CH=CHCH=CHCOOH)不是同系物,它们与足量的氢气充分反应后的产物也不是同系物 | |
| D. | 等物质的量的乙炔、乙醛、(HO)CH2-CH2(OH)完全燃烧时的耗氧量相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
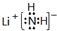 .
. CH2CH3(g)?催化剂
CH2CH3(g)?催化剂 CH=CH2(g)+H2(g)
CH=CH2(g)+H2(g)
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 )是一种名贵的香料,又是合成VE、VA、紫罗兰酮、胡萝卜素等的中间体.合成芳樟醇的一种方法如下:
)是一种名贵的香料,又是合成VE、VA、紫罗兰酮、胡萝卜素等的中间体.合成芳樟醇的一种方法如下: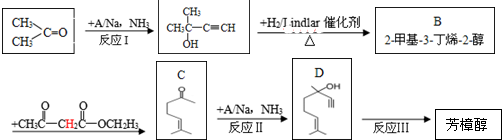
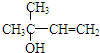 ,C分子中的官能团名称为羰基、碳碳双键,已知反应I和反应Ⅱ的原子利用率100%,则A的结构简式为HC≡CH.
,C分子中的官能团名称为羰基、碳碳双键,已知反应I和反应Ⅱ的原子利用率100%,则A的结构简式为HC≡CH.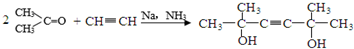 .
. ,写出柠檬醛的另一种同分异构体的结构简式(不改变分子中原子的连接方式)
,写出柠檬醛的另一种同分异构体的结构简式(不改变分子中原子的连接方式)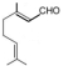 ;芳樟醇在H+作用下也可异构化为香叶醇(
;芳樟醇在H+作用下也可异构化为香叶醇(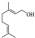 ).下列有关柠檬醛的下列说法正确的是BCD
).下列有关柠檬醛的下列说法正确的是BCD查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ;三溴化磷
;三溴化磷 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅蓄电池放电过程中,正极质量增加,负极质量减小 | |
| B. | 反应NH4Cl(s)=NH3(g)+HCl(g)在室温下不能自发进行,则该反应的△H>0 | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 | |
| D. | 0.1 mol•L-1 CH3COOH溶液加水稀释后,溶液中c(OH-)、CH3COOH浓度均减少 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com