
【题目】I.人们应用原电池原理制作了多种电池,以满足不同的需要,广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格。
(1)铅蓄电池在放电时发生的电池反应式为:Pb+PbO2+2H2SO4=2PbSO4+2H2O。正极电极反应式为_________。电池工作一段时间后需要充电,充电过程中电池液中H2SO4的浓度_____(填“增大”、“减小”或“不变”)。
⑵某学习小组依据氧化还原反应:2Ag++Cu===Cu2++2Ag设计成原电池,则负极发生的电极反应为___________;当反应进行到一段时间后取出电极材料,测得某一电极增重了 5.4g,则该原电池反应共转移了的电子数目是________________________。
⑶燃料电池是一种高效、环境友好的供电装置,如图是电解质为稀硫酸溶液的氢氧燃料电池原理示意图,回答下列问题:
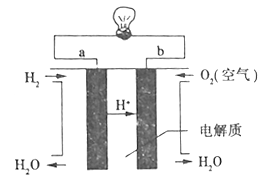
①该电池的正极反应式_________________。
②若该电池的效率80%,当外电路通过0.2mo1电子时,消耗O2的体积____L(标准状况)
II.用Cl2生产某些含氯有机物时会产生副产物HC1。利用反应4HC1+O2 ![]() 2Cl2+2H2O,可实现氯的循环利用。己知上述反应中,4mol HC1被氧化,放出约116kJ的热量。
2Cl2+2H2O,可实现氯的循环利用。己知上述反应中,4mol HC1被氧化,放出约116kJ的热量。
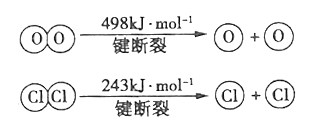
计算断开1 mol H-O键与断开1 mol H-C1键断所吸收能量相差约为______kJ。
【答案】 PbO2+4H++SO42-+2e-=PbSO4+2H2O 增大 Cu-2e=Cu2+ 0.05NA O2+4e+4H+=2H2O 1.4 32
【解析】I.(1)放电时,负极电解反应:Pb-2e-+SO42-=PbSO4 ,正极电极反应:PbO2+2e-+4H++2SO42-=PbSO4+2H2O,根据电池反应式知,充电时硫酸是生成物,所以充电过程中电池液中H2SO4的浓度增大;
⑵由反应“2Ag++Cu═Cu2++2Ag”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,反应式为Cu-2e-=Cu2+;当银电极质量增加5.4g,则n(Ag)=![]() =0.05mol,根据电极反应Ag++e-=Ag,可知导线中通过的电子的物质的量为0.05mol;
=0.05mol,根据电极反应Ag++e-=Ag,可知导线中通过的电子的物质的量为0.05mol;
⑶①氢氧燃料电池,通氧气的极为正极,发生还原反应,该电池的正极反应式O2+4e+4H+=2H2O;
②设参加反应的氧气为VL(标准状况),则![]() ×80%×4mol=0.2mol,解得V=1.4;
×80%×4mol=0.2mol,解得V=1.4;
II.E(H-O)、E(HCl)分别表示H-O键能、H-Cl键能,反应A中,4mol HCl被氧化,放出115.6kJ的热量,反应热△H=反应物总键能-生成物的总键能,故:4×E(H-Cl)+498kJ/mol-[2×243kJ/mol+4×E(H-O)]=-115.6kJ/mol,整理得,4E(H-Cl)-4E(H-O)=-127.6kJ/mol,即E(H-O)-E(HCl)=31.9kJ/mol,
故断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ/mol×1mol=31.9kJ≈32kJ。
。


科目:高中化学 来源: 题型:
【题目】已知:①2H2(g)+O2(g)=2H2O(l);△H=-572kJ/mol
②2H2(g)+O2(g)=2H2O(g);△H=-484kJ/mol
③CH4(g)+2O2(g)=2H2O(l)+CO2(g);△H=-890kJ/mol
(1)已知H-H的键能436kJ/molO=O的键能496kJ/molH-O的键能463kJ/mol,根据上述数据计算①②哪一个反应可以通过键能直接计算得出 。并计算写出反应 H2O ( l ) = H2O ( g )的焓变△H= 。
(2)请根据题干计算CO2(g)+4H2( g ) =CH4( g ) +2H2O( g )的焓变△H= 。
(3)在①②③三个方程式中哪一个是燃烧热的热化学方程式 。(填反应方程式的序号)标准状况下,取甲烷和氢气的混合气体11.2 L完全燃烧后恢复到常温,则放出的热量为263.8kJ,试求混合气体中甲烷和氢气体积比 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期主族元素X、Y、Z、W的原子序数依次增大。化合物甲由X、Y、Z三种元素组成,25℃时,0.01mol·L-1甲溶液中的![]() ;Z与W同周期,且W的最高正价与最低负价的代数和为4。下列说法中正确的是
;Z与W同周期,且W的最高正价与最低负价的代数和为4。下列说法中正确的是
A. 原子半径:X<Y<Z<W
B. 最简单氢化物的稳定性:Y>W
C. Z分别与Y、W组成的化合物中化学键类型均相同
D. 粘有W的单质的试管可用酒精洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】升高温度时,化学反应速率加快,主要是由于
A. 分子运动速率加快,使反应物分子间的碰撞机会增多
B. 反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多,化学反应速率加快
C. 该化学反应的过程是放热的
D. 该化学反应的过程是吸热的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类合理的是
A.碱性氧化物:Na2O、CaO、Mn2O7、Na2O2
B.碱:NaOH、KOH、Ba(OH)2、Na2CO3
C.铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3·H2O
D.氧化物:CO2、NO、SO2、H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是重要的有机合成中问体,以A为原料合成香料M和线型高分子树脂N的路线如图所示(部分反应条件和物质略去):

已知:
①A是芳香烃的含氧衍生物,其蒸气密度是相同条件下氢气密度的54倍。
②有机物分子中,同一个碳原子上连接两个—OH不稳定,会自动失水。
③ (R、R′表示烃基或氢原子)。
(R、R′表示烃基或氢原子)。
请回答:
(1)A的化学名称为________。N的结构简式为________。
(2)D中含氧官能团的名称为________。C的分子中最多有________个原子共平面。
(3)B→C时,第一步转化的反应类型为________。
(4)E→M的化学方程式为________。
(5)L是D的一种同系物,比D少1个碳原子且存在顺反异构;核磁共振氢谱中有6种吸收峰。则L的顺式结构简式为________。
(6)同时满足下列条件的E的同分异构体有________种(不考虑立体异构),任写其中一种的结构简式________。
①苯环连有两个取代基
②能发生银镜反应
③能与NaHCO3反应生成CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】⑴写出N2的电子式__________。下列能实现人工固氮的是__________。
A.闪电 B.在加压降温的条件下使空气中的氮气液化
C.根瘤 D.合成氨车间
⑵实验室通常用加热消石灰与氯化铵固体的方法来制取氨气。
写出该反应的化学方程式________________________________________。
实验室制取氨气的方法有多种,下面的装置和选用的试剂中错误的是__________。

⑶氨气可使湿润的红色石蕊试纸变蓝的原因(用化学用语表示)
____________________________________________________________
⑷用乙装置吸收一段时间氨后,再通入空气,同时将加热的铂丝插入乙 装置的锥形瓶内,锥形瓶中不可能生成的物质是:__________。
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
写出乙装置中氨催化氧化的化学方程式:_____________________。
⑸已知![]() ,常温常压下,在一密闭容器中将
,常温常压下,在一密闭容器中将![]() 和
和![]() 充分反应后,剩余气体的体积为__________
充分反应后,剩余气体的体积为__________ ![]() 。
。
⑹在标准状况下, ![]() 水中可溶解
水中可溶解![]() ,所得溶液的密度为
,所得溶液的密度为![]() ,则氨水的物质的量浓度为__________
,则氨水的物质的量浓度为__________ ![]() (保留一位小数)。
(保留一位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种白色固体可能由![]() 离子中的若干种组成, 陶宝同学设计实验检验其组成,记录如下:
离子中的若干种组成, 陶宝同学设计实验检验其组成,记录如下:
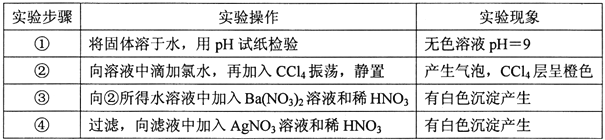
下列关于固体组成的结论错误的是
A. 肯定含有![]() 和
和![]() B. 至少含有
B. 至少含有![]() 中的一种离子
中的一种离子
C. 肯定不含Ba2+,一定含有Cl- D. 无需焰色反应即可断定溶液中含有Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com