
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g)![]() 2Z(g),此反应达到平衡状态的标志是
2Z(g),此反应达到平衡状态的标志是
A. 容器内气体密度不随时间变化
B. 容器内气体的平均相对分子质量不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 消耗0.1 mol X的同时生成0.2 mol Z
【答案】B
【解析】
由X(g)+2Y(g)![]() 2Z(g)可知,该反应前后的化学计量数之和不等,然后根据达到平衡时,正逆反应速率相等,但不等于零,各物质的浓度不再改变判断。
2Z(g)可知,该反应前后的化学计量数之和不等,然后根据达到平衡时,正逆反应速率相等,但不等于零,各物质的浓度不再改变判断。
A.反应前后气体的总质量不变,容器体积也没变,所以密度一直不变,则密度不随时间变化不是平衡化学平衡状态的依据,A错误;
B.该反应为反应前后气体分子数不相等的可逆反应,若反应未达到平衡,气体的物质的量发生变化,由于气体总质量不变,所以气体平均摩尔质量就会发生变化,若反应达到平衡,气体的物质的量不变,气体平均摩尔质量也就不变,因此可根据容器内气体的平均相对分子质量不随时间变化判断反应达到平衡状态,B正确;
C.反应达平衡时的浓度与反应初始物质的量及反应的转化率有关,因此不能确定是否达到平衡,B错误;
D.无论反应是否达到化学平衡,消耗的反应物与反应生成的生成物的物质的量之比等于方程式中相应的化学计量数之比,所以不能用来作为判断是否达到平衡状态的依据,D错误;
故合理选项是B。


科目:高中化学 来源: 题型:
【题目】将0.1 mol MnO2和100 mL 12 mol·L-1盐酸混合后缓缓加热,生成气体单质A,反应完全后向留下的溶液中加入足量AgNO3溶液 (不考虑盐酸的挥发) 。下列说法错误的是
A.在生成气体A的反应中,MnO2是氧化剂,盐酸是还原剂
B.气体单质A是氯气,它的体积是2.24L
C.生成AgCl沉淀的物质的量为1mol
D.整个反应过程被氧化的盐酸有0.4mol,并转移了0.2mol e-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuBr是一种白色晶体,见光或潮湿时受热易分解,在空气中逐渐变为浅绿色。实验室制备CuBr的反应原理为:SO2+2CuSO4+2NaBr+ 2H2O=2CuBr↓+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的的是

A. 用装置甲制取SO2 B. 用装置乙制取CuBr
C. 用装置丙避光将CuBr与母液分离 D. 用装置丁干燥CuBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有反应4HCl(g)+O2(g)═2Cl2(g)+2H2O(g),已知2 mol O2被还原时,放出a kJ的热量,且知断开1 mol O=O键需要吸收b kJ的热量,断开1 mol Cl—Cl键需要吸收c kJ的热量。则断开1 mol H—O键比断开1 mol H—Cl键所需能量高
A. (b-a-2c)/4kJB. (a+2b-4c)/8kJC. (a+b-2c)/4kJD. (2b-a-4c)/8kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在373K时,把0.1mol![]() 气体通入体积为lL的恒容密闭容器中,立即出现红棕色。在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法错误的是
气体通入体积为lL的恒容密闭容器中,立即出现红棕色。在60s时,体系已达平衡,此时容器内压强为开始时的1.6倍。下列说法错误的是
A. 压缩容器,颜色加深
B. 在平衡时体系内含![]() 0.04mol
0.04mol
C. 以![]() 的浓度变化表示的平均反应速率为0.001mol/(L·s)
的浓度变化表示的平均反应速率为0.001mol/(L·s)
D. 平衡时,如果再充入一定量![]() ,则可提高
,则可提高![]() 的转化率
的转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来,加“碘”食盐中添加较多的是碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极材料,以KI溶液为电解液,在一定条件下进行电解,反应的化学方程式为KI+3H2O![]() KIO3+3H2↑。下列有关说法不正确的是
KIO3+3H2↑。下列有关说法不正确的是
A. 加碘食盐不能使淀粉溶液变蓝
B. 电解时,石墨作阳极,不锈钢作阴极
C. 阳极的电极反应式为I-+3H2O+6e-=IO3-+6H+
D. 转移3 mol电子,理论上可制得107 g KIO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4溶液是中学化学及工农业生产中常见的一种试剂。
(1)某同学配制CuSO4溶液时,向盛有一定量硫酸铜晶体的烧杯中加入适量的蒸馏水,并不断搅拌,结果得到悬浊液。他认为是固体没有完全溶解,于是对悬浊液加热,结果发现浑浊更明显了。原因是(用离子方程式和简要文字说明表示)___________________________,最后,他向烧杯中加入了一定量的_________________溶液,得到了澄清的CuSO4溶液。
(2)该同学利用制得的CuSO4溶液,进行了以下实验探究。
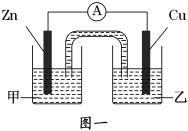
①图一是根据反应Zn+CuSO4═Cu+ZnSO4设计成的锌铜原电池。电解质溶液乙是______溶液,Cu极的电极反应式是____________________。
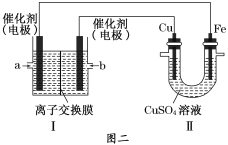
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为NaOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则Fe电极为__________(填“阳极”或“阴极”)。若铜电极的质量减轻3.2 g,则消耗的CH4在标准状况下的体积为___________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写不正确的是
A.向CaCl2 溶液中通入少量CO2气体:Ca2+ + CO2 + H2O=CaCO3↓ + 2H+
B.大理石与醋酸反应:CaCO3 + 2CH3COOH= Ca2+ + 2CH3COO-+ H2O + CO2↑
C.制备Fe(OH)3胶体:Fe3+ + 3H2O![]() Fe(OH)3(胶体)+ 3H+
Fe(OH)3(胶体)+ 3H+
D.少量碳酸氢钠溶液与足量石灰水反应:Ca2+ + OH-+ HCO3-=CaCO3↓ + H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com