
铁及其化合物是中学化学中的一类重要物质,下列关于铁元素的叙述中正确的是 ( )。
A.2Fe3++Fe===3Fe2+成立说明氧化性:Fe3+>Fe2+
B.25 ℃,pH=0的溶液中,Al3+、NH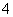 、NO
、NO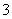 、Fe2+可以大量共存
、Fe2+可以大量共存
C.5.6 g铁与足量的氯气反应失去电子为0.2 mol
D.硫酸亚铁溶液中加入过氧化氢溶液:Fe2++2H2O2+4H+===Fe3++4H2O
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
下列关于卤素的叙述正确的是 ( )。
①卤素的钾盐中,最易被氧化的是氟化钾 ②溴中溶有少量氯气,可以用加入溴化钠再用汽油萃取的方法提纯 ③溴化银具有感光性,碘化银不具有感光性 ④某溶液与淀粉KI溶液反应出现蓝色,则证明该溶液是氯水或溴水 ⑤氟气跟氯化钠水溶液反应,一定有氟化氢和氧气生成 ⑥氯气跟水反应时,水既不是氧化剂也不是还原剂
A.①③⑤ B.②③⑥
C.②⑤⑥ D.①③④
查看答案和解析>>
科目:高中化学 来源: 题型:
现有含MgCl2、AlCl3均为n mol的混合溶液,向其中滴NaOH溶液至过量。加入NaOH的物质的量与生成沉淀的物质的量的关系正确的是(离子形成沉淀或沉淀的溶解与溶液pH的关系如下表) ( )。
| 离子 | Mg2+ | Al3+ | 物质 | Al(OH)3 |
| 开始沉淀时的pH | 8.93 | 3.56 | 开始溶解时的pH | 8.04 |
| 完全沉淀时的pH | 10.92 | 4.89 | 完全溶解时的pH | 12.04 |

查看答案和解析>>
科目:高中化学 来源: 题型:
某同学设计了如下实验测量m g铜银合金样品中铜的质量分数:

下列说法中不正确的是 ( )。
A.合金的熔点比其成分金属低,通常比成分金属具有更优良的金属特性
B.铜银都能与稀硝酸反应,收集到的V L气体可能全为NO
C.操作Ⅰ是过滤,操作Ⅱ是洗涤,操作Ⅲ应是烘干
D.根据反应收集到的气体体积可以计算铜和银的质量分数
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
A.Fe在一定条件下与水反应生成H2和Fe(OH)3
B.Fe3O4溶于盐酸后加入几滴KSCN溶液,溶液显血红色
C.FeCl2溶液蒸干灼烧后得到FeCl2固体
D.将FeCl3饱和溶液滴入NaOH溶液中可制备Fe(OH)3胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况。
| 步骤 | 操作 | 现象 |
| Ⅰ | 向2 mL 1 mol·L-1 FeCl3溶液中加入一定量的Na2SO3溶液 | 溶液由棕黄色变为红褐色,并有少量刺激性气味的气体逸出 |
(1)常温下,FeCl3溶液的pH________7(填“<”、“>”或“=”)。
(2)分析红褐色产生的原因。
①甲同学认为步骤I中溶液呈红褐色是因为生成了Fe(OH)3,请用化学平衡移动原理解释溶液呈红褐色的原因:___________________________。
②乙同学认为可能是发生了氧化还原反应,其中Fe3+→Fe2+;请写出Fe3+跟SO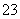 反应的离子方程式_____________________________________________
反应的离子方程式_____________________________________________
________________________________________________________。
乙同学查阅资料得知:
| 1.Fe2+与SO 2.墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色。 |
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| Ⅱ | 用激光笔照射步骤I中的红褐色溶液 | 出现“丁达尔效应” |
甲同学因此得出结论:溶液呈红褐色是因为生成了Fe(OH)3。而乙同学认为甲同学得出结论的证据仍然不足,乙同学的理由是________。
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| Ⅲ | 向1 mol·L-1的FeCl3溶液中通入一定量的SO2 | 溶液由黄色变为红褐色 |
| Ⅳ | 用激光笔照射步骤Ⅲ中的红褐色溶液 | 没有出现“丁达尔效应” |
①经检验步骤Ⅲ中红褐色溶液含有Fe2+,检验Fe2+选用的试剂是________(填字母)。
a.K3[Fe(CN)6]溶液 b.KSCN溶液 c.KMnO4溶液
②请用离子方程式和必要的文字说明步骤Ⅲ中出现红褐色的原因____________________。
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确。
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有a mol AlCl3的溶液中加入含b mol KOH的溶液,生成沉淀的物质的量可能是 ( )。
①a mol ②b mol ③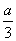 mol ④
mol ④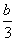 mol ⑤0 mol ⑥(4a-b) mol
mol ⑤0 mol ⑥(4a-b) mol
A.①②④⑥ B.①③④⑤⑥
C.②③⑤⑥ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
钠是很活泼的金属,在空气中燃烧的产物是Na2O2。Na2O的制取可以通过如下反应完成:Na+NaNO3 Na2O+N2↑(未配平)。请回答下列问题:
Na2O+N2↑(未配平)。请回答下列问题:
(1)上述反应的氧化剂是________(写化学式)。制取Na2O时,若金属钠与NaNO3按质量比23∶17投料,充分反应后收集到的气体体积为1.12 m3(标准状况下),则制得的Na2O的质量为________ kg。
(2)制取Na2O时由于设备密封性不好而进入了少量空气,导致制得的Na2O产品中含有Na2O2杂质。现有Na2O产品m g(假设只含有Na2O2杂质),请从下面选用合适的仪器和试剂,设计一种可选用的实验仪器组合,以完成样品中Na2O含量的测定。

可选用的试剂:
a.浓硫酸 b.水 c.盐酸标准溶液 d.NaOH标准溶液
e.酚酞 f.碱石灰 g.稀盐酸
| 实验过程中发生反应的化学方程式 | 实验所需仪器(用字母表示) | 实验所需试剂(用字母表示) | 实验需直接测定的有关物理量(用文字说明) |
(3)某学生设计了以下实验方案来测定该试样中Na2O的质量分数,其操作流程和实验数据如下:




该Na2O产品中Na2O的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在某一溶液中,含有NH+4、I—、Ba2+、Cl—等离子,则该溶液的pH和介质可以是
A.pH=12,氨水为介质 B.pH=8,次氯酸钠溶液为介质
C.pH=3,H2SO4溶液为介质 D.pH=l,稀硝酸为介质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com