
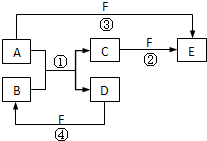
 A��B��C��D��E��F�������ʵ��ת����ϵ��ͼ��ʾ����Ӧ����δ����������з�Ӧ�����û���Ӧ��
A��B��C��D��E��F�������ʵ��ת����ϵ��ͼ��ʾ����Ӧ����δ����������з�Ӧ�����û���Ӧ�� Si+2CO�����ʴ�Ϊ��SiO2+2C
Si+2CO�����ʴ�Ϊ��SiO2+2C Si+2CO����
Si+2CO����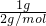 =0.5mol ʱ���ų�92.3kJ����������H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��
=0.5mol ʱ���ų�92.3kJ����������H2��g��+Cl2��g��=2HCl��g����H=-184.6KJ/moL��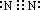 ��NH3��������Ӧ����NO��ˮ��Ϊ��ҵ������ķ�Ӧ����ѧ����ʽΪ
��NH3��������Ӧ����NO��ˮ��Ϊ��ҵ������ķ�Ӧ����ѧ����ʽΪ 4NO+6H2O��
4NO+6H2O��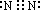 ��4NH3+5O2
��4NH3+5O2  4NO+6H2O��
4NO+6H2O�� 4NO2��+CO2��+2H2O��
4NO2��+CO2��+2H2O�� 4NO2��+CO2��+2H20��
4NO2��+CO2��+2H20�� 4NO2��+CO2��+2H2O��
4NO2��+CO2��+2H2O��

 ��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
��ͼͼ�麮����ҵ������ҵ���ִ�ѧ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ������ | X | Y | Z |
| �۵�/K | 1266 | 1534 | 183 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 [��ѧ/ѡ��/���ʽṹ������]A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������Ԫ�ض�Ӧ�ĵ��ʾ�Ϊ���壮A��C��E��Ԫ�ص�ԭ�Ӻ����ֻ��2��δ�ɶԵ��ӣ�B��EԪ�ص�ԭ������֮�͵���C��DԪ�ص�ԭ������֮�ͣ�
[��ѧ/ѡ��/���ʽṹ������]A��B��C��D��E���ֶ�����Ԫ�أ�ԭ��������������Ԫ�ض�Ӧ�ĵ��ʾ�Ϊ���壮A��C��E��Ԫ�ص�ԭ�Ӻ����ֻ��2��δ�ɶԵ��ӣ�B��EԪ�ص�ԭ������֮�͵���C��DԪ�ص�ԭ������֮�ͣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com