
 ̽��ʵ�鷢�֣����ᷢ��������ԭ��Ӧʱ��Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�ͣ�
̽��ʵ�鷢�֣����ᷢ��������ԭ��Ӧʱ��Ũ��Խϡ����Ӧ��ԭ�����е�Ԫ�صĻ��ϼ�Խ�ͣ�

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
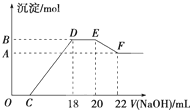
| A������AΪSO2��H2�Ļ���� |
| B����Ӧ�й�����Zn 65 g |
| C������A��SO2��H2�������Ϊ1��4 |
| D����Ӧ�й�ת��3 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1��1 | B��1��2 |
| C��2��1 | D��3��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2��8��18��32��32��18��8 |
| B��2��8��18��32��50��8 |
| C��2��8��18��32��18��8 |
| D��2��8��18��32��50��18 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ||
A��b=
| ||
B��b��
| ||
C��b��
| ||
D��b��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������һ�������ɸ�CH2ԭ���ŵ��л���֮�以��Ϊͬϵ�� |
| B�������ӽṹ�в����ڶ�����̼̼˫������˱����ܷ����ӳɷ�Ӧ |
| C���ɷ��ӹ��ɵ����ʣ����Ӽ���������Ӱ�����ʵ��۷е���ܽ��Ե���Ҫ����֮һ |
| D���������������ԭ�Ӵ���ͬһ��ƽ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com