
在一定条件下,把一定量NH3充入容积固定的密闭容器中,发生反应2NH3 (g) 3H2(g)+N2(g)。达到平衡时,若保持温度不变,增加N2的浓度。下列说法正确的是
3H2(g)+N2(g)。达到平衡时,若保持温度不变,增加N2的浓度。下列说法正确的是
A.平衡向正反应方向移动 B.化学平衡常数不变
C.化学平衡常数增大 D.化学平衡常数减小
科目:高中化学 来源: 题型:
1g氢气燃烧生成液态水放出142.9 kJ热量,表示该反应的热化学方程式正确的是
A.2H2(g) + O2(g) = 2H2O(l) △H =-142.9 kJ/mol
B.H2(g) + 1/2O2(g) = H2O(l) △H =-285.8 kJ/mol
C.2H2 + O2 = 2 H2O △H =-571.6 kJ/mol
D.H2(g) + 1/2O2(g) = H2O(g) △H = -285.8kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
现有可逆反应m A(g)+ n B(g) 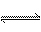 x C(g);ΔH = a kJ/mol。该反应在不同温度和压强条件下,反应物A的转化率的变化情况如图所示。下列判断正确的是
x C(g);ΔH = a kJ/mol。该反应在不同温度和压强条件下,反应物A的转化率的变化情况如图所示。下列判断正确的是
 A.a < 0,m+n < x
A.a < 0,m+n < x
B.a < 0,m+n > x
C.a > 0,m+n < x
D.a > 0,m+n > x
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 molA气体和2molB气体在2L的容器中混合,一定条件下发生如下反应:2A(g)+B(g)=2C(g)若经2s(秒)后测得C的浓度为0.6mol·L-1 ,下列说法正确的是
A.2 s 时物质 A 的转化率为70%
B.用物质 B 表示的反应的平均速率为 0.6 mol·L-1·s-1
C.用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1
D.2 s 时物质 B 的浓度为 0.6 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
对于反应2SO2(g)+O2(g) 2SO3(g),能增大正反应速率的措施是
2SO3(g),能增大正反应速率的措施是
A. 增大容器容积 B.通入大量O2 C.移去部分SO3 D.降低体系温度
查看答案和解析>>
科目:高中化学 来源: 题型:
可逆反应mA(固)+nB(气)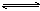 e C(气)+f D(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是
e C(气)+f D(气),反应过程中,当其它条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如下图:下列叙述正确的是
A.达平衡后,加入催化剂则C%增大
B.达平衡后,增加A的量有利于平衡向右移动
C.化学方程式中n>e+f
D.达平衡后,若升温,平衡左移
查看答案和解析>>
科目:高中化学 来源: 题型:
“中和热的测定”实验步骤为:
① 准备反应装置(如右图)。
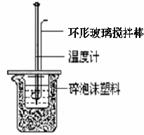
② 用一个量筒量取40 mL 0.50 mol/L盐酸,倒入小烧杯中,并用温度计测量盐酸的温度,记录。然后把温度计上的酸用水冲洗干净。
③ 用另一个量筒量取40 mL 0.55 mol/LNaOH溶液,并用温度计测量NaOH溶液的温度,记录。
④ 把温度计和_____________________放入小烧杯的盐酸中,并把量筒中的NaOH溶液一次倒入小烧杯(注意不要洒到外面)。用环形玻璃搅拌棒轻轻搅动溶液,并准确读取混合溶液的最高温度。
⑤_____________________________________________________________________。
⑥ 根据实验数据计算中和热。
请回答下列问题
(1)补全第④步中所缺仪器__________________。
(2)补全第⑤步操作步骤__________________。
(3)第②步如果不把温度计上的酸用水冲洗干净直接测量NaOH溶液的温度,则测得的ΔH__________________。(填“偏大”“偏小”或“无影响”)。
(4)近似认为0.50 mol/L盐酸0.55 mol/LNaOH溶液的密度都是1g/mL,中和后生成的溶液的比热容c=4.18J/(g·℃),起始平均温度为t1℃,反应后最高温度为t2℃,则中和热(不用化简):
ΔH=__________________。
(5)0.50L 1.00 mol/L H2SO4溶液与1.00 L 1.00 mol/L NaOH溶液完全反应,放出57.16kJ的热量,写出该中和反应的热化学方程式
__________________________________________________________________。
(6)_______(填“能”或“不能”)用稀Ba(OH)2和稀硫酸代替盐酸和NaOH溶液,理由是____________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中微粒的物质的量浓度关系正确的是( )
A.氯水中:c(Cl2)=2c(ClO-)+2c(Cl-)+2c(HClO)
B.Na2CO3溶液:c(OH-)+c(H+)=c(HCO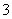 )+2c(H2CO3)
)+2c(H2CO3)
C.等浓度的NaClO、NaHCO3混合溶液中:c(HClO)+c(ClO-)=c(HCO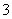 )+c(H2CO3)
)+c(H2CO3)
D.室温下,向0.01 mol·L-1 NH4HSO4溶液中滴加NaOH溶液至中性:
c(Na+)>c(SO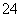 )>c(NH
)>c(NH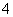 )>c(OH-)=c(H+)
)>c(OH-)=c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
食品干燥剂应无毒、无味、无腐蚀性及环境友好。下列说法错误的是
A.硅胶可用作食品干燥剂
B.P2O5不可用作食品干燥剂
C.六水合氯化钙可用作食品干燥剂
D.加工后具有吸水性的植物纤维可用作食品干燥剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com