
| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(2b-a)kJ•mol-1 | |
| B. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(b-a)kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2b-a)kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=-(2b+a)kJ•mol-1 |
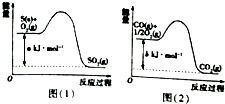
分析 图1:S(s)+O2(g)=SO2(g)△H1=-aKJ/mol
图2:CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2=-bKJ/mol;
依据盖斯定律②×2-①得到,由此分析解答.
解答 解:图1:S(s)+O2(g)=SO2(g)△H1=-aKJ/mol
图2CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H2=-bKJ/mol;
依据盖斯定律②×2-①得到:SO2(g)+2CO(g)=S(s)+CO2(g)△H=2△H2-△H1=-(2b-a)KJ/mol,
故选A.
点评 考查了反应热的问题,对学生综合运用知识能力有一定的要求,特别是根据图中信息热化学方程式,要求学生有较好从图中获取信息的能力,整个题目难度较大.


 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温时在水中的溶解性:NaHCO3>Na2CO3 | |
| B. | 热稳定性:NaHCO3<Na2CO3 | |
| C. | 与酸反应的快慢:NaHCO3<Na2CO3 | |
| D. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 增大压强,化学反应速率一定加快 | |
| B. | 其它条件不变,温度越高,反应速率越快 | |
| C. | 同时改变两个变量来研究反应速率的变化,能更快得出有关规律 | |
| D. | 增加反应物的量,反应速率一定加快 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中富集含微量元素的化合物 | B. | 使含微量元素的离子沉淀 | ||
| C. | 对含微量元素的混合物进行提纯 | D. | 从化合物中冶炼这些单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NO2、Cl2O7都是酸性氧化物 | B. | 水银、水玻璃都是混合物 | ||
| C. | 干冰、可燃冰都是分子晶体 | D. | HD、HCHO都是极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

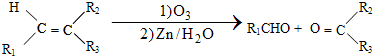
 $\stackrel{一定条件}{→}$R-N=C
$\stackrel{一定条件}{→}$R-N=C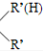 +H2O
+H2O .
.
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
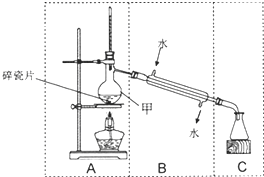 如图装置在中学化学实验中常用于物质的分离与提纯.
如图装置在中学化学实验中常用于物质的分离与提纯.| A.除去CO2气体中混有的少量HCl气体 |
| B.从硝酸钾和氯化钠的混合物中提纯得到硝酸钾 |
| C.用含有Fe3+的自来水获得少量纯净的水 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com