
| A.取少量样品放入试管中,加热,试管口放一团蘸有无水硫酸铜粉末的棉花团,变蓝则可证明晶体的成分中含有结晶水 |
| B.取少量样品溶于水,得淡绿色溶液,滴入2滴KSCN溶液,溶液不显红色,再滴入几滴新制氯水,溶液变为红色,则可证明晶体的成分中含有Fe2+ |
| C.取少量样品溶于水,加少量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- |
| D.取少量样品放入试管中,加入少量稀NaOH溶液,在试管口用湿润的红色石蕊试纸检验,则可证明晶体的成分中是否含有NH4+ |
科目:高中化学 来源:不详 题型:实验题
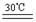 CO(NH2)2·H2O2。过氧化尿素的部分性质如下:
CO(NH2)2·H2O2。过氧化尿素的部分性质如下:| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2?H2O2 | 白色晶体 | 45℃ | 75~85℃ | 易溶于水、有机溶剂 |

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙酸和乙酸乙酯可用Na2CO3溶液加以区别 |
| B.戊烷(C5H12)有两种同分异构体 |
| C.乙烯、聚氯乙烯和苯分子均含有碳碳双键 |
| D.糖类、油脂和蛋白质均可发生水解反应 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置 |
| B.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 |
| C.制乙烯时,用排水法或向上排空气法收集气体 |
| D.制二氧化氮时,用水或NaOH溶液吸收尾气 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.沉淀a为AgC1 | B.沉淀b为BaCO3 |
| C.气体中含有SO2 | D.气体中没有HC1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
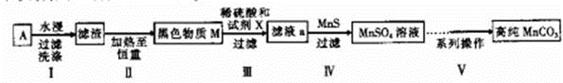
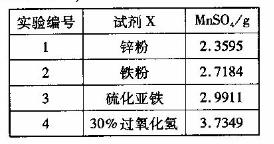
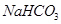 、乙醇)
、乙醇)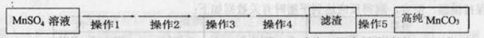
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
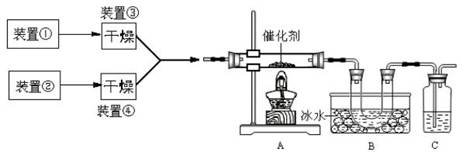

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com