
ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ�飨ͼ��a��b��c��ʾֹˮ�У���
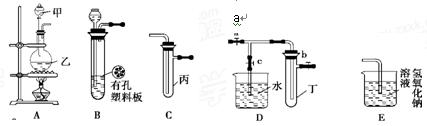
�밴Ҫ����գ�
��1������Bװ�ÿ���ȡ�������� ��
��2��A��C��E�������װ�ÿ�������ȡCl2��������ص�����ʵ�顣
�����ڱ��м�������ˮ�������Ƶ���ˮ����������ˮ�ֳ����ݣ����Т�����ʵ�飬ʵ�����������������£�
| ʵ����� | ʵ����� | ���� | ���� |
| �� | ����ˮ����Ʒ����Һ | ��Һ��ɫ | ������ˮ��Ӧ�IJ�����Ư���� |
| �� | ��ˮ�м��� NaHCO3��ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ�IJ�����н�ǿ������ |
��������ʵ���Ľ����Ƿ������������������˵�����ɡ�
![]() ��
��
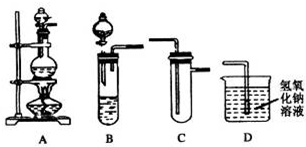
������������װ�����һ����ʵ�飬��֤Cl����Br���Ļ�ԭ��ǿ�����ֱ�ָ���ס��ҡ�����ʢװ���Լ���ʵ�������ۣ�
![]() ��
��
��3��B��D��Eװ����������B��ʢװŨ�����ͭƬ�������п����ϰ��ϣ������Ƶ�NO2
�������й�ʵ�顣
B�з�����Ӧ�Ļ�ѧ����ʽΪ ��
�� ����Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ�� ���ٴ�ֹˮ�� ��ʹ�ձ��е�ˮ�����Թܶ��IJ����� ��
�� �Թܶ��е�NO2��ˮ��ַ�Ӧ�������Թ��ڻ���ͨ��һ������O2��ֱ���Թ�ȫ������ˮ����������Һ�����ʵ����ʵ���Ũ���� �����尴��״�����㣩��
��1��H2��CO2��H2S�� ��1�֣�
��2����ʵ�����ۺ�����1�֣���ʵ�����۲���������Ϊ��ȡ�������к���HCl���壬HCl����ˮ������NaHCO3��ĩ��Ӧ�������ݣ�2�֣�?
���ڼס��ҡ����зֱ�װ��Ũ���ᡢMnO2��NaBr��Һ����ƿ���л���ɫ�������ɣ��Թ�����Һ����ɫ��Ϊ��ɫ��֤��Cl2��������ǿ��Br2,��֤��Br-�Ļ�ԭ��ǿ��Cl-��
�������Լ���ʵ�������۸�1�֣�
��3����Cu+4HNO3(Ũ) ��Cu(NO3)2+2NO2��+2H2O ��2�֣�
�� a b c ��1�֣� ˫�ֽ��գ����ȣ��Թܶ�ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ���2�֣�
��0.045 mol��L-1����д��1/22.4 mol��L-1��2�֣�δд��λ��1�֣�


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

| ʵ�� | ʵ����� | ���� | ���� |
| I | ����ˮ����Ʒ����Һ | Ʒ����Һ��ɫ | ������ˮ��Ӧ�IJ������Ư���� |
| �� | ��ˮ�м���̼�����Ʒ�ĩ | ����ɫ���ݲ��� | ������ˮ��Ӧ�IJ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ʵ�� ��� |
ʵ����� | ���� | ���� |
| �� | ����ˮ����Ʒ����Һ | Ʒ����Һ��ɫ | ������ˮ��Ӧ�IJ�����Ư���� |
| �� | ��ˮ�м���̼�����Ʒ�ĩ | ����ɫ������� | ������ˮ��Ӧ�IJ���������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ����� | ʵ�鲽�� |
| �� | ��þ����ɰֽ��ĥ�����ˮ�У�������Һ�еμӷ�̪��Һ |
| �� | �����Ƶõ���Na2S��Һ�еμ����Ƶ���ˮ |
| �� | ��һС������Ʒ�����з�̪��Һ����ˮ�� |
| �� | ��þ��Ͷ��ϡ������ |
| �� | ������Ͷ��ϡ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
| ||
| ||
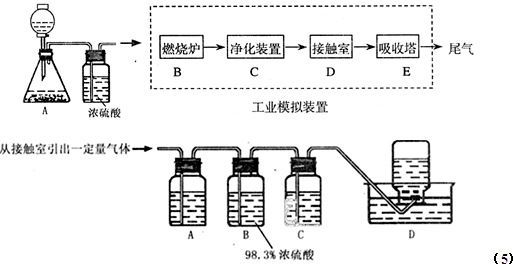
| ѹǿ/Mpa ת���� �¶�/�� |
0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com