

| ||
| ||
| ||
| ||


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
| A、二价金属,二元酸 |
| B、二价金属,三元酸 |
| C、三价金属,二元酸 |
| D、一价金属,一元酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②④ | B、①③⑤⑦ |
| C、①④⑥⑧ | D、②④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 铜及其化合物在生活、生产中有广泛应用.请回答下列问题:
铜及其化合物在生活、生产中有广泛应用.请回答下列问题:
| ||
| c(Cu2+) |
| c(Ca2+) |
| KSP(CuCO3) |
| KSP(CaCO3) |
| c(Cu2+) |
| c(Ca2+) |
| KSP(CuCO3) |
| KSP(CaCO3) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、反应物的总能量大于生成物的总能量 |
| B、该反应遵循“能量守恒定律” |
| C、该反应中,化学能只转变成热能 |
| D、断开1mol H-H键和1mol Cl-Cl键所吸收的总能量小于形成2mol H-Cl键所放出的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
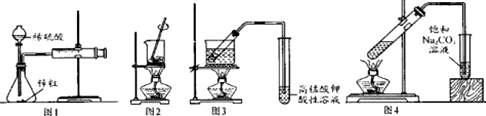
| A、图1--测量锌与硫酸反应的速率 |
| B、图2--灼烧海带成海带灰 |
| C、图3--验证溴乙烷与NaOH乙醇溶液反应生成乙烯 |
| D、图4--实验室制备收集乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com