
【题目】下列各组中的离子能够大量共存于同一溶液中的是 ( )
A. CO32-、Ba2+、Na+、NO3- B. H+、Al3+、OH-、SO42-
C. OH-、NO3-、K+、Na+ D. K+、Fe3+、Cl-、OH-
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A.1L0.1mol·L—1的氨水中含有的NH3分子数为0.1NA
B.标准状况下,2.24L的CCl4中含有的C—Cl键数为0.4NA
C.常温常压下,3.0g含甲醛的冰醋酸中含有的原子总数为0.4 NA
D.常温常压下,Na2O2与足量CO2反应生成2.24L O2,转移电子数为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝的叙述不正确的是
A. 铝是地壳中含量最多的元素
B. 在常温下,铝能与NaOH溶液反应
C. 铝是一种比较活泼的金属
D. 在化学反应中,铝容易失去电子,是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)芒硝的化学式是_________________。
(2)以氯化钠、石灰石、水为原料制取漂白粉,写出有关反应的化学方程式。
①______________________________;②_________________________________;
③______________________________;④_________________________________。
(3)元素铬(Cr)在溶液中主要以Cr3+、Cr2O72—(橙红色)、CrO42—(黄色)CrO2—等形式存在。回答下列问题:
①![]() 与
与![]() 的化学性质相似。写出向
的化学性质相似。写出向![]() 溶液中加入过量
溶液中加入过量![]() 溶液反应的离子方程式_____________________________________________。
溶液反应的离子方程式_____________________________________________。
②![]() 价铬的化合物毒性较大,常用
价铬的化合物毒性较大,常用![]() 将废液中的
将废液中的![]() 还原成
还原成![]() ,该反应的离子方程式为 ______________________________________________________。
,该反应的离子方程式为 ______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组对物质的性质进行相关探究. 【提出问题】氯化氢(HCl)气体显酸性吗?
【进行实验】该兴趣小组的同学根据二氧化碳与水反应的实验探究方法,用三朵由紫甘蓝的汁液染成蓝紫色的纸质干燥小花进行如图1的三个实验: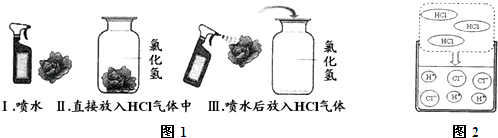
实验现象:Ⅰ和Ⅱ中小花不变色;Ⅲ中小花变红色.
【查阅资料】图2是同学们查阅的氯化氢气体溶于水的微观示意图.
【实验结论】氯化氢气体不显酸性.
【交流反思】
(1)从微观角度分析氯化氢气体不显酸性的原因是 .
(2)小明向实验Ⅲ中变红的小花上喷适当过量的稀氢氧化钠溶液,发现小花最后变成黄绿色,写出相关反应的化学方程式 .
(3)紫甘蓝的汁液在酸性溶液中显色,在碱性溶液中显色.
(4)下列实验可以用来说明氯化氢气体不显酸性的是 .
A.测试盐酸的导电性,盐酸能导电
B.干燥的碳酸钠粉末放人氯化氢气体中,不反应
C.氢气与氯气反应,生成氯化氢气体
D.干燥的碳酸钠粉末放人盐酸中,能反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列制备金属单质的方法或原理正确的是
A.在高温条件下,用H2还原MgO制备单质Mg
B.在通电条件下,电解熔融Al2O3制备单质Al
C.在通电条件下,电解饱和食盐水制备单质Na
D.加强热,使CuO在高温条件下分解制备单质Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生产、生活中产生的废水、废气是环境污染的重要源头。在环境治理方面人们可利用I2O5和Na2SO3等化工产品实现对废水和废气的治理。
(1)利用I2O5的氧化性处理废气H2S,得到S、I2两种单质,发生反应的化学方程式为________________。
(2)利用I2O5也可消除CO的污染,其反应原理为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s) ΔH。已知在不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
5CO2(g)+I2(s) ΔH。已知在不同温度(T1、T2)下,向装有足量I2O5固体的2 L恒容密闭容器中通入2 mol CO,测得CO2气体的体积分数φ(CO2)随时间t的变化曲线如图所示。
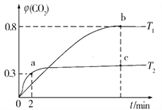
①温度为T2时,0~2 min 内,CO2的平均反应速率 υ(CO2)=______________。
②b点时CO的转化率为_______,化学反应的平衡常数K=_____(填表达式)。
③反应:I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)的ΔH______0(填“>”“<”或“=”)。
5CO2(g)+I2(s)的ΔH______0(填“>”“<”或“=”)。
④上述反应在T1下达到平衡时,再向容器中充入物质的量均为2 mol的CO和CO2气体,则化学平衡________(填“向左” “向右”或“不”)移动。
⑤下列现象,可以表示上述反应达到平衡状态的是____________(填字母)。
A.容器内的压强不再变化 B.混合气的平均相对分子质量不再变化
C.混合气的密度不再变化 D.单位时间内消耗CO和生成CO2的物质的量之比为1∶1
(3)Na2SO3具有还原性,其水溶液可以吸收Cl2(g),减少环境污染。
已知反应:
①Na2SO3(aq)+Cl2(g)+H2O(l) ![]() Na2SO4(aq)+2HCl(aq) ΔH1=a kJ·mol1
Na2SO4(aq)+2HCl(aq) ΔH1=a kJ·mol1
②Cl2(g)+H2O(l) ![]() HCl(aq)+HClO(aq) ΔH2=b kJ·mol1
HCl(aq)+HClO(aq) ΔH2=b kJ·mol1
试写出Na2SO3(aq)与HClO(aq)反应的热化学方程式:________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质结构概念的判断正确的是( )
A.离子键:阴阳离子间的静电吸引作用
B.离子化合物:只含离子键的物质
C.共价键:通过共用电子对产生的作用
D.共价化合物:含有共价键的物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。已知:KMnO4+ 16HC1=2KCl+5Cl2↑ +2MnCl2+8H2O,向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。

下列有关说法正确的是
A. a处变蓝、b处变棕红说明非金属性:C12> Br2 > I2
B. c处先变红、后褪色说明Cl2与H2O反应生成HC1
C. d处立即褪色说明Cl2与H2O反应生成HCIO
D. e处变红说明Cl2与Fe2+反应生成Fe3+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com