
【题目】下列离子方程式正确的是( )
A.将Ca(HCO3)2溶液与少量Ca(OH)2溶液混合:Ca2+ +OH + HCO3 = CaCO3↓+ H2O
B.向Ba(NO3)2溶液中通入SO2气体,出现白色沉淀:SO2+H2O+Ba2+ = BaSO3↓+ 2H+
C.碳酸钙溶于醋酸:CaCO3 + 2H+ = Ca2+ + CO2↑+ H2O
D.往苯酚钠溶液中通入少量CO2:2![]() +CO2+H2O2
+CO2+H2O2![]() +CO32
+CO32
【答案】A
【解析】
A选项,将Ca(HCO3)2溶液与少量Ca(OH)2溶液混合,少的定为1mol,1mol Ca(OH)2电离出2mol氢氧根和1mol钙离子,2mol氢氧根消耗2mol碳酸氢根反应生成2mol碳酸根,和2mol钙离子反应生成2mol碳酸钙,因此Ca2+ +OH + HCO3 = CaCO3↓+ H2O,故A正确;
B选项,向Ba(NO3)2溶液中通入SO2气体,出现白色沉淀,二氧化硫被硝酸根氧化生成硫酸钡,故B错误;
C选项,醋酸是弱酸,不能拆,故C错误;
D选项,往苯酚钠溶液中通入少量CO2只能生成碳酸氢根,![]() +CO2+H2O2
+CO2+H2O2![]() +HCO3,故D错误。
+HCO3,故D错误。
综上所述,答案为A。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】密闭容器中,反应A(g)+2B(g)![]() C(g)分别在三种不同的实验条件下进行,它们的起始浓度分别为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1、c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法正确的是( )
C(g)分别在三种不同的实验条件下进行,它们的起始浓度分别为c(A)=0.100mol·L-1、c(B)=0.200mol·L-1、c(C)=0mol·L-1,反应物A的浓度随时间的变化如图所示。下列说法正确的是( )
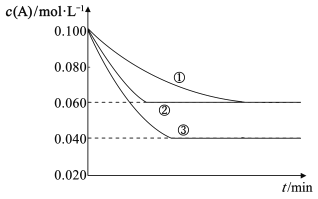
A.与①比较,②可能加入了催化剂
B.与①比较,③一定是增大了压强
C.实验③平衡时B的转化率为40%
D.该反应一定有ΔH>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将17.6克Fe2O3和Cu的混合物溶解于足量的稀盐酸中,再加铁粉9.8克,待铁粉溶解后,溶液中无Fe3+,此过程共产生2.24升H2(标况),则下列判断正确的是
A.混合物中Cu全部被氧化为Cu2+以后,Cu2+又全部被还原
B.混合物中Cu全部被氧化为Cu2+以后,Cu2+又部分被还原
C.混合物中Cu部分被氧化为Cu2+以后,Cu2+又全部被还原
D.混合物中Cu部分被氧化为Cu2+以后,Cu2+又部分被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向浓度相等、体积均为100 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,逐滴加入0.1 mol/L的盐酸,产生CO2的体积(标准状况)与所加盐酸的体积关系如图所示。
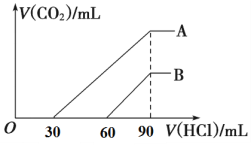
(1)A曲线表明,原溶液通入CO2 ________mL(标准状况)。
(2)B曲线表明,原溶液通入CO2后,所得溶液中溶质的物质的量之比为__________。
(3)原NaOH溶液的物质的量浓度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
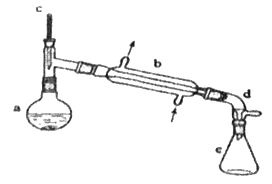
【题目】分离提纯是化学实验中的重要部分,方法有过滤、蒸发、萃取、蒸馏等,应用广泛,环己醇脱水是合成环己烯的常用方法,实验室合成环己烯的反应和实验装置如图:
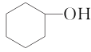
![]()
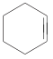 +H2O
+H2O
可能用到的有关数据如下:
相对分子质量 | 密度(g/cm3) | 沸点/℃ | 溶解性 | |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
Ⅰ.合成反应:在a中加入20 g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1 mL浓硫酸,b中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90 ℃。
Ⅱ.分离提纯:反应粗产物倒入分液漏斗中分别用少量5 %碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙,最终通过蒸馏得到纯净环己烯10 g。
回答下列问题:
(1)装置b的名称是__。
(2)加入碎瓷片的作用是__;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是__(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)分液漏斗在使用前须清洗干净并__;在本实验分离过程中,产物应该从分液漏斗的__(填“上口倒出”或“下口倒出”)。
(4)分离提纯过程中加入无水氯化钙的目的是__。
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有__(填正确答案标号)。
A.蒸馏烧瓶 B.温度计 C.分液漏斗 D.牛角管 E.锥形瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A~I分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出)。已知H为固态氧化物,F是红褐色难溶于水的沉淀,且A、B、C、D、E、F六种物质中均含同一种元素。

请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含的同一种元素的名称是________。
(2)反应①的化学方程式为_____________________________________
反应③的离子方程式为________________________
反应⑧的化学方程式为_____________________________________
(3)反应⑥过程中的现象是______________________________。
(4)1molI发生反应后生成的A高温下与足量的水蒸气反应,生成的气体换算成标准状况下占______L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钴铁氧体(CoFe2O4)不仅是重要的磁性材料、磁致伸缩材料,还是重要的锂离子电池负极材料。工业上,可以由废旧锂钴电池正极材料(主要含Fe、Al、硅等杂质)回收钴,再用电化学法制得CoFe2O4。其流程如图所示(过程中所加试剂均足量)
Ⅰ.废旧电池中钴的回收
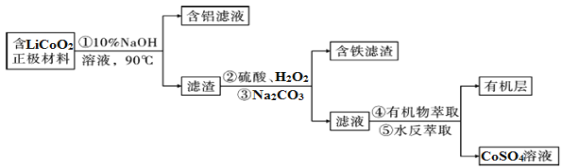
(1)写出过程②中LiCoO2与H2O2发生反应的化学方程式:__________________________。
(2)过程③Na2CO3的主要作用为__________________。
Ⅱ.电解法制得钴铁合金
(3)配制0.050molL1FeSO4和0.025molL1CoSO4的混合溶液,用铜作阴极、石墨作阳极进行电解,获得CoFe2合金。阴极的电极方程式为:___________。
Ⅲ.阳极氧化法制得钴铁氧体
(4)以1.500molL1NaOH溶液作电解液,纯净的钴铁合金(CoFe2)作阳极进行电解,在阳极上获得CoFe2O4薄膜。该电解过程的化学方程式为__________________________。
(5)当电路上有0.4mol电子转移时,阳极电极材料增重质量为3.4g,与理论值不符,其原因可能为_______________。
(6)由废旧锂钴电池制CoFe2O4的现实意义在于:_____(写一条即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,10L密闭容器中加入5molSO2、3molO2,反应达平衡时有3molSO2发生了反应。试填写下列空格:
(1)生成SO3 ____________ mol;
(2)O2的转化率为____________;
(3)平衡时体系中SO2的百分含量(体积分数)为____________;
(4)降低温度,O2的转化率____________;v正____________;(填“增大”、“减小”或“不变”)
(5)保持容器体积不变,加入He,则SO2的物质的量____________。(填“增大”、“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用CH4可消除NO2的污染,反应原理为:CH4(g)+2NO2(g)![]() N2(g) + CO2(g) +2H2O(g),在10L密闭容器中分别加入0.50mol CH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:
N2(g) + CO2(g) +2H2O(g),在10L密闭容器中分别加入0.50mol CH4和1.2molNO2,测得不同温度下n(CH4)随时间变化的有关实验数据如表所示:

下列说法正确的是
A.组别①中0 ~20 min内,NO2降解速率为0.0125molL-1min-1
B.由实验数据可知温度T1<T2
C.40min时,表格中M对应的数据为0.18
D.该反应只有在高温下才能自发进行
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com