
|
已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式为: C(s)+O2(g) 2H2(g)+O2(g) CO(g)+ 则下列说法或方程式书写不正确的是 | |
| [ ] | |
A. |
C(s)的燃烧热ΔH=-393.5 kJ/mol |
B. |
H2(g)的燃烧热ΔH=-242.0 kJ/mol |
C. |
C(s)+ |
D. |
2H2(g)+O2(g) |
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源:山西省“晋商四校”2011-2012学年高二下学期联考化学试题 题型:058
氨在国民经济中占有重要的地位,2008年,我国氨产量接近500万吨.下图是合成氨的简要流程.

(1)天然气、重油、煤都可以与水反应制得氢气.下表是某合成氨厂采用不同原料的相对投资和能量消耗.
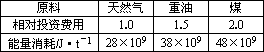
①依据上表信息,你认为采用________为原料最好.
②请写出甲烷在高温、催化剂的作用下与水蒸气反应生成氢气和一氧化碳的化学方程式:________.
③已知C(s)、CO(g)和H2(g)完全燃烧的热化学方程式分别为:C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol-1;
2CO(g)+O2(g)=2CO2(g) ΔH=-566 kJ·mol-1;
2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ·mol-1;
试写出由C与水蒸气在高温条件下反应生成氢气与一氧化碳的热化学方程式________.
(2)下表是在某种催化剂作用下用体积比为1:3的氮、氢混合气反应应达到平衡时的一些实验数据.
①依据表中数据判断,合成氨反应N2+3H2![]() NH3的△H________0(填“>”、“<”或“无法判断”),请简要说明理由________;
NH3的△H________0(填“>”、“<”或“无法判断”),请简要说明理由________;

②该反应的化学平衡常数表达式为________.
③在300℃、10 MPa下,合成氨反应达到平衡时,混合气体的体积是反应开始时的________倍.
查看答案和解析>>
科目:高中化学 来源:2011—2012学年辽宁省沈阳二中高二上学期10月月考化学试卷 题型:单选题
下列说法正确的是
| A.已知:2H2(g)+O2(g)=2H2O(l)△H<0,反应物总能量小于生成物总能量 |
| B.测定盐酸和氢氧化钠反应的中和热实验中,所用试剂可以是浓溶液 |
| C.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则1molH2SO4和1molBa(OH)2反应放出的热量为114.6kJ |
| D.已知C(s)与CO(g)的燃烧热分别为393.5kJ·mol-1 、283.0kJ·mol-1,则相同条件下C(s)与O2(g)反应生成1molCO(g)的反应热为△H=-110.5kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
科目:高中化学 来源:专项题 题型:填空题




 2NH3的 △H____________0(填“>”“<”或“无法判断”),请简要说明理由______________。
2NH3的 △H____________0(填“>”“<”或“无法判断”),请简要说明理由______________。 查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com