
【题目】从某些性质看,NH3和H2O,NH4 +和H3O+,OH-和NH2-,N3—和O2—两两相似,据此判断下列反应式中不正确的是
A. 2Na+2NH3===2NaNH2+H2↑
B. 3CaO+4NH4Cl===Ca3N2+2NH3↑+3H2O+4HCl
C. 3Mg(NH2)2![]() Mg3N2+4NH3↑
Mg3N2+4NH3↑
D. NH4Cl+NaNH2===NaCl+2NH3↑
【答案】B
【解析】由题意知,NH3和H2O,NH4 +和H3O+,OH-和NH2-,N3—和O2—两两相似。类比2Na+2H2O===2NaOH+H2↑,可知2Na+2NH3===2NaNH2+H2↑可以发生;类比CaO+2HCl===CaCl2+2H2O,可知CaO+2 NH4Cl ===CaCl2+2H2O+2NH3↑可以发生、3CaO+4NH4Cl===Ca3N2+2NH3↑+3H2O+4HCl不可以发生;类比Mg(OH)2![]() MgO+H2O↑,可知3Mg(NH2)2
MgO+H2O↑,可知3Mg(NH2)2![]() Mg3N2+4NH3↑可以发生;类比HCl+NaOH===NaCl+H2O,可知NH4Cl+NaNH2===NaCl+2NH3↑可以发生。综上所述,B不正确,本题选B。
Mg3N2+4NH3↑可以发生;类比HCl+NaOH===NaCl+H2O,可知NH4Cl+NaNH2===NaCl+2NH3↑可以发生。综上所述,B不正确,本题选B。


科目:高中化学 来源: 题型:
【题目】由葡萄糖发酵可得乳酸,为研究乳酸的分子组成和结构,进行了下述实验:
(1)称取乳酸0.90g,在某种状况下使其完全气化,相同状况下同体积的H2的质量为0.02g,则乳酸的相对分子质量为 .
(2)若将上述乳酸蒸气在氧气中燃烧只生成CO2和H2O(g),当全部被碱石灰吸收时,碱石灰的质量增加1.86g;若将此产物通入过量石灰水中,则产生3.00g白色沉淀.则乳酸的分子式为 .
(3)另取0.90g乳酸,若与足量金属钠反应,生成H2224mL(标准状况),若与足量碳酸氢钠反应,生成224mLCO2(标准状况),则乳酸的结构简式可能为或 .
(4)若葡萄糖发酵只生成乳酸,其反应的化学方程式为 .
(5)乳酸与乙酸、乳酸与乙醇均能发生酯化反应,相同质量乳酸所生成的两种酯化产物(有机物)的质量比为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨广泛用于生产化肥、制冷剂等方面。回答下列问题:
(1)实验室可用下图所示装置合成氨。
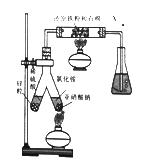
①合成氨时,还原铁粉的作用是________________。
②锥形瓶中盛有一定量的水,并滴有几滴酚酞试剂,反应—段时间后,锥形瓶中溶液变红,则气体X的成分为N2、水蒸气、____________和_________________。
⑵最近斯坦福大学研究人员发明了一种SUNCAT的锂循环系统,可持续合成氨,其原理如图所示。
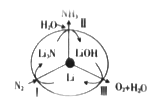
①图中反应Ⅱ的化学方程式为____________________。
②反应Ⅲ中能量转化的方式是__________________(填“电能转变为化学能”或“化学能转变为电能”)。
(3)液氨可用作制冷剂,液氨气化时__________(填“释放”或“吸收”)能量;液氨泄漏遇明火会发生爆炸。已知部分化学键的键能数据如下表所示:
共价键 | N-H | O=O | N≡N | O-H |
键能/kJ·mol-1 | 391 | 498 | 946 | 463 |
则反应 4NH3(g)+3O2(g)=2N2(g)+6H2O(g)的反应热△H=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表前四周期的一部分,关于元素X、Y、Z的叙述错误的是

A. X的气态氢化物与Y的最高价氧化物的水化物能反应生成盐
B. 等物质的量浓度的X、Y、Z的气态氢化物的水溶液的pH:X>Y>Z
C. Z的单质常温下是液体,可与铁粉反应
D. Z的原子序数比Y大9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验室制备乙酸乙酯的操作错误的是( )
A. 配料:加入过量乙醇B. 加热:用水浴加热
C. 分离:用边反应边分离的方法D. 净化:产物用氢氧化钠溶液洗涤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.1 L水中溶解了58.5 g NaCl,该溶液的物质的量浓度为1 mol/L
B.从1 L 2 mol/L的H2SO4溶液中取出0.5 L,该溶液的浓度为1 mol/L
C.配制480 mL 0.5 mol/L的CuSO4溶液,需62.5 g胆矾
D.10 g 98%的硫酸(密度为1.84 gcm﹣3)与10 mL18.4 molL﹣1的硫酸的浓度不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO、NOx等)的污染是重要的科学研究课题。
(1)一定条件下的密闭容器中,进行反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g),下列说法不能说明该反应达到平衡的是____(填字母)。
N2(g)+2CO2(g),下列说法不能说明该反应达到平衡的是____(填字母)。
A.NO的生成速率与NO的消耗速率相等 B.υ(CO)=υ(CO2)
C.体系的压强保持不变 D.各物质的浓度保持不变
(2)可用活性炭还原法处理氮氧化物。有关反应的化学方程式为:C(s)+2NO(g)![]() N2(g)+CO2(g)△H>0某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g)△H>0某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测得各物质的浓度如下:
浓度/mol·L﹣1 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
①写出该反应的平衡常数表达式:K=____________________。
②30min后,改变某一条件,平衡发生了移动,则改变的条件是_______________;若升高温度,NO浓度将_______(填“增大”、“不变”或“减小”)。
③计算从0~20min内,NO的平均反应速率为___________________。
(3)在一定温度和压强下,CO和H2催化合成二甲醚的反应为:3H2(g)+3CO(g)![]() CH3OCH3(g)+CO2(g),若一体积可变的密闭容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。则:反应开始时正、逆反应速率的大小:υ(正)____υ(逆)(填“ >”、“ < ”或“=”)。
CH3OCH3(g)+CO2(g),若一体积可变的密闭容器中充入3 mol H2、3 mol CO、1 mol CH3OCH3、1 mol CO2,经一定时间达到平衡,并测得平衡时混合气体密度是同温同压下起始时的1.6倍。则:反应开始时正、逆反应速率的大小:υ(正)____υ(逆)(填“ >”、“ < ”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com