
| A. | CO2 | B. | N2O5 | C. | PCl5 | D. | NaCl |
分析 CO2、N2O5、PCl5分子中某原子最外层电子数=元素原子最外层电子数+该元素原子化合价绝对值,若该值等于8,则该原子满足8电子结构,NaCl为离子化合物无分子存在.
解答 解:A.CO2为共价化合物,CO2分子中C元素化合价为+4,C原子最外层电子数是4,4+4=8,所以碳原子满足8电子结构,O元素化合价为-2,O原子最外层电子数是6,6+2=8,C、O原子均满足8个电子稳定结构,故A正确;
B.N2O5中N元素化合价为+5,N原子最外层电子数是5,5+5=10,O元素化合价为-2,原子最外层电子数为6,所以6+2=8,分子中N原子不满足8电子结构,故B错误;
C.PCl5中Cl元素化合价为-1,Cl原子最外层电子数是7,1+7=8,P元素化合价为+5,P原子最外层电子数为5,所以5+5=10,分子中P原子不满足8电子结构,故C错误;
D.NaCl为离子化合物无分子存在,故D错误;
故选A.
点评 本题考查共价键,注意对8电子结构判断,分子中含有氢元素,该分子一定不满足各原子达8电子结构,离子化合物无分子存在,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 由硫酸铁溶液与硫酸铵溶液按一定比例混合后蒸发结晶而得 | |
| B. | 此溶液中与下列粒子可以大量共存:H+、SO42-、I-、C6H5OH | |
| C. | 此溶液中离子浓度大小关系为:SO42->Fe3+>H+>OH- | |
| D. | 将含0.1 molNH4Fe(SO4)2溶液中滴加0.1 molBa(OH)2,反应的离子方程式为:Fe3++2SO42-+2Ba2++3OH-=2BaSO4↓+Fe(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10℃20 mL 3mol/L的X溶液 | B. | 20℃30 mL 2molL的X溶液 | ||
| C. | 20℃10 mL 4mol/L的X溶液 | D. | 10℃10 mL 2mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 符合同一通式的物质 | |
| B. | 含有相同官能团的物质 | |
| C. | 相对分子质量相差14或者14的倍数的物质 | |
| D. | 通式为CnH2n+2,且C原子数不相等的物质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
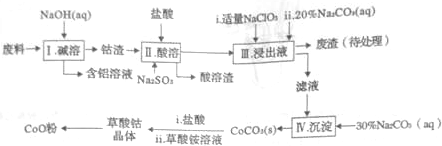
| Fe3+ | Co2+ | Co3+ | Al2+ | |
| pH(开始沉淀) | 1.9 | 7.15 | -0.23 | 3.4 |
| pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
| 温度范围/℃ | 固体质量/g |
| 150~210 | 4.41 |
| 290~320 | 2.41 |
| 890~920 | 2.25 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 加成、水解、加成、消去 | B. | 取代、水解、取代、消去 | ||
| C. | 加成、取代、取代、消去 | D. | 取代、取代、加成、氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com