
【题目】I 在稀氨水中分别加入下列各种物质:A 氨气、 B纯水、C少量浓硫酸、 D少量氢氧化钠固体、 E少量硫酸铝固体 (用字母填空)
(1)能使c(OH-)减少,使c(NH4+)增大的是_________________。
(2)能使c(OH-)增大,使c(NH4+)减小的是_________________。
(3)能使c(OH-)和c(NH4+)都增大的是________________________。
(4)能使c(OH-)和c(NH4+)都减小的是________________________。
II 硒酸(H2SeO4)在水溶液中的电离如下:
H2SeO4===H++HSeO![]() ,HSeO
,HSeO![]()
![]() H++SeO
H++SeO![]() ,K2=1.0×10-2(25 ℃)。向H2SeO4溶液中滴加少量氨水,该反应的离子方程式为______________________。
,K2=1.0×10-2(25 ℃)。向H2SeO4溶液中滴加少量氨水,该反应的离子方程式为______________________。
III 常温下0.1 mol·L-1的CH3COOH溶液在加水稀释过程中,下列表达式的数据一定变小的是________(填序号)。
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-) D.![]()
若该溶液升高温度,上述4种表达式的数据增大的是_________________________。
【答案】 C、E D A B H++NH3·H2O===NH![]() +H2O A ABCD
+H2O A ABCD
【解析】I、氨水中存在NH3H2ONH4++OH-。
①加入少量硫酸或硫酸铝,可生成水或氢氧化铝沉淀,使平衡向正向移动,则c(OH-)减少、c(NH4+)增大,故答案为:CE;
②能使c(OH-)增大、c(NH4+)减少,应加入碱或水解呈碱性的物质,则NaOH溶液以及少量K2CO3符合,故答案为:D;
③通入氨气,可使c(OH-)和c(NH4+)都增大,故答案为:A;
④加水稀释时,可使c(OH-)和c(NH4+)都减少,故答案为:B;
II、氨水少量,所以硒酸(H2SeO4)的第一步完全电离产生的氢离子过量,所以反应的离子方程式为:H++NH3H2O=NH4++H2O,故答案为:H++NH3H2O=NH4++H2O;
III 、A.CH3COOH溶液加水稀释过程中,由于溶液体积增大,而醋酸的电离程度较小,则稀释后溶液中c(H+)减小,故A正确;B.稀释过程中氢离子的物质的量增大、醋酸的物质的量减小,由于在同一溶液中,溶液体积相同,则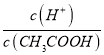 的比值增大,故B错误;C.溶液中c(H+)c(OH-)之积为水的离子积,稀释后溶液温度不变,则水的离子积不变,故C错误;D.
的比值增大,故B错误;C.溶液中c(H+)c(OH-)之积为水的离子积,稀释后溶液温度不变,则水的离子积不变,故C错误;D. 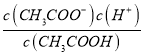 为醋酸电离平衡常数表达式,平衡常数只随温度变化,不随浓度变化,故比值不变,故D错误;故选A;若该溶液升髙温度,促进CH3COOH、H2O电离平衡正向进行,溶液中氢离子浓度、醋酸根离子浓度增大,A.氢离子浓度增大;B.
为醋酸电离平衡常数表达式,平衡常数只随温度变化,不随浓度变化,故比值不变,故D错误;故选A;若该溶液升髙温度,促进CH3COOH、H2O电离平衡正向进行,溶液中氢离子浓度、醋酸根离子浓度增大,A.氢离子浓度增大;B. 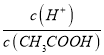 比值增大;C.溶液中c(H+)c(OH-)之积为水的离子积,升温促进水电离,离子积常数增大;D.
比值增大;C.溶液中c(H+)c(OH-)之积为水的离子积,升温促进水电离,离子积常数增大;D. 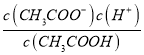 为平衡常数表达式升温促进电离平衡常数增大;上述4种表达式的数据增大的是ABCD,故答案为:A;ABCD。
为平衡常数表达式升温促进电离平衡常数增大;上述4种表达式的数据增大的是ABCD,故答案为:A;ABCD。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】元素R,X,T,Z,Q在元素周期表中的相对位置如表所示,其中只有X是短周期的金属元素,下列判断正确的是( ) 
A.X的最高价氧化物能不溶于强碱
B.非金属性:T<R
C.气态氢化物稳定性:T>Z
D.R与Q的原子核外电子数相差16
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】奥运五环代表着全世界五大洲的人民团结在一起.下列各项中的物质能满足如图中阴影部分关系的是( ) 
A.①NaCl;②K2SO4;③KCl;④(NH4)2SO4;
B.①Na2SO4;②K2SO4;③KCl;④(NH4)2SO4;
C.①NaCl;②K2SO4;③KCl;④NH4Cl;
D.①Na2SO4;②K2SO4;③KCl;④NH4Cl.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】等质量镁铝合金分别与下列四种过量的溶液充分反应,放出H2最多的是( )
A. H2SO4溶液 B. NaOH溶液 C. 蔗糖溶液 D. NaCl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 我国是个钢铁大国,钢铁产量为世界第一,高炉炼铁是最为普遍的炼铁方法。
I.已知:2CO(g)+O2(g)=2CO2(g) △H =-566kJ/mol
2Fe(s)+![]() O2(g)=Fe2O3(s) △H =-825.5 kJ/mol
O2(g)=Fe2O3(s) △H =-825.5 kJ/mol
则,(1)反应:Fe2O3(s)+3CO(g)![]() 2Fe(s)+3CO2(g) △H =____________。
2Fe(s)+3CO2(g) △H =____________。
(2)反应 ![]() Fe2O3(s)+CO(g)
Fe2O3(s)+CO(g)![]()
![]() Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在
Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在
一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过l0min后达到平衡,则CO的平衡转化率=____________。
II.高炉炼铁产生的废气中的CO可进行回收,使其在一定条件下和H2反应制备甲醇:![]() 。请根据图示回答下列问题:
。请根据图示回答下列问题:

(1)从反应开始到平衡,用H2浓度变化表示平均反应速率v(H2)= ____________![]() △H =____________。
△H =____________。
(2)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:

则下列关系正确的是 ____________。
A c1=c2 B.2Q1=Q3 C. 2a1=a3
D. a1 +a2 =1 E. 该反应若生成1mol CH3OH,则放出(Q1+Q2)kJ热量
(3)若在一体积可变的密闭容器中充入l molCO、 2mol H2和1mol CH3OH,达到平衡吋测得混合气体的密度是同温同压下起始的1.6倍,则该反应向____________ (填“正”、“逆”)反应方向移动。
III.在一个密闭容器中,有一个左右可滑动隔板,两边分别进行可逆反应,各物质的物质的量分别如下:M、N、P为2.5mol、3.0mol、1.0mol。A、C、D各为0.50mol,B的物质的量为x mol,当x在一定范围内变化,均可以通过调节反应器的温度,使两侧反应均达到平衡,且隔板在反应器的正中位置。达到平衡后,测得M的转化率为75%,填写空白:
![]()
(1)达到平衡后,反应器左室气体总的物质的量为____________mol。
(2)若要使右室反应开始时V正>V逆,x的取值范围____________。
(3)若要使右室反应开始时V正逆,x的取值范围____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋中含有乙酸,下列关于乙酸的说法中正确的是 ( )
A.乙酸是有刺激性气味的液体B.一个乙酸分子中含有4个氢原子,它不是一元羧酸
C.乙酸在常温下就很容易发生酯化反应D.乙酸酸性较弱,不能使石蕊溶液变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工业废水中含有Fe2+、Cu2+、SO42-及少量的Na+,现为了回收FeSO4晶体及Cu,设计了如下流程:

回答下列问题:
(1)C是________, A、B、D中属于混合物的是_________。
(2)操作I是_______,加入A时发生的离子方程式为_________。
(3)操作III包括蒸发浓缩,冷却结晶,过滤,洗涤,干燥。蒸发时需要的仪器(不含夹持仪器)除酒精灯外还有______、________,蒸发溶液时,待_________(填现象)时停止加热。
(4)过滤所得的晶体需用冰水洗涤,用冰水的目的是_______;洗涤后继续用无水乙醇洗涤,用乙醇的目的是_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
①CH3OH(g)+H2O(g)=CO2(g)+3H2(g); △H= +49.0 kJ·mol-1
②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);△H= -192.9 kJ·mol-1
下列说法正确的是
A. CH3OH的燃烧热为192.9 kJ·mol-1
B. 反应①中的能量变化如图所示

C. CO2和H2转变成CH3OH的过程不一定要吸收能量
D. 根据②推知反应:CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的△H<-192.9kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电池叙述正确的是( )
A.水果电池是高效环保的家用电池B.锌锰干电池是一种常用的二次电池
C.锌锰干电池碳棒是负极,锌片是正极D.锌锰干电池工作一段时间后锌外壳逐渐变薄
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com