
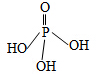
 (1)三聚磷酸可视为三个磷酸分子(磷酸的结构如图)之间脱去两个分子的产物,其结构式为
(1)三聚磷酸可视为三个磷酸分子(磷酸的结构如图)之间脱去两个分子的产物,其结构式为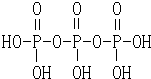 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.分析 (1)一个磷酸中的羟基与另一个磷酸的氢之间可以脱水,据此来书写三聚磷酸的结构式,三聚磷酸钠(俗称“五钠”)即把三聚磷酸中的羟基氢原子均被钠原子代替的产物;
(2)根据盖斯定律进行计算.
解答 解:(1)一个磷酸中的羟基与另一个磷酸的H之间可以脱水.结构式则为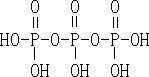 ,“五钠”即五个钠原子,所以三聚磷酸钠的化学式为Na5P3O10,
,“五钠”即五个钠原子,所以三聚磷酸钠的化学式为Na5P3O10,
故答案为:Na5P3O10;
(2)根据盖斯定律得Cl2(g)+PCl3(g)=PCl5(g)△H=$\frac{b-a}{4}$KJ•mol-1,利用Cl2(g)+PCl3(g)=PCl5(g)△H=$\frac{b-a}{4}$KJ•mol-1,可得E(Cl-Cl)+3×1.2c-5c=$\frac{b-a}{4}$,因此可得E(Cl-Cl)=$\frac{b-a+5.6c}{4}$kJ•mol-1,由P4是正四面体可知P4中含有6个P-P键,由题意得6E(P-P)+10×$\frac{b-a+5.6c}{4}$-4×5c=b,解得E(P-P)=$\frac{5a-3b+12c}{12}$kJ•mol-1,
故答案为:$\frac{5a-3b+12c}{12}$kJ•mol-1.
点评 本题主要根据盖斯定律等知识点来分析解答即可,难点是(4)中P-P键键能的计算,题目难度中等.


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O | |
| B. | Na放入水中,产生气体:Na+H2O=Na++OH-+H2↑ | |
| C. | 实验室用大理石和稀盐酸制取CO2:2H++CO32-=CO2↑+H2O | |
| D. | 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH-=Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:F>Na>Mg>Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2CO3<H3PO4<H2SO4 | D. | 碱性强弱:KOH>NaOH>Mg(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
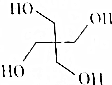 季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )
季戊四醇被大量用于涂料工业生产醇酸树脂、合成高级润滑剂、增塑剂、表面活性剂以及医药、炸药等,其结构简式如图所示.季戊四醇可由HCHO与CH3CHO两种有机物按一定比例加成得到的产物与H2再加成得到.则反应中HCHO与CH3CHO的物质的量之比为( )| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| X | Y | |
| Z | W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com