
| A£® | CH3CH2CHO | B£® | CH3CH2COOH | C£® | CH3COCH3 | D£® | CH3CH2OCH3 |
·ÖĪö øł¾Ż1-±ū“¼ÕōĘųÓėæÕĘų»ģŗĻĶعżČČĶĶų£¬Éś³ÉµÄ»ÆŗĻĪļĪŖ±ūČ©£ŗCH3CH2CHO£¬ŌŁĄūÓĆ·Ö×ÓŹ½ĻąĶ¬µ«½į¹¹²»Ķ¬Ą“ÅŠ¶ĻÓėŃ”Ļī»„ĪŖĶ¬·ÖŅģ¹¹Ģå½ųŠŠÅŠ¶Ļ£®
½ā“š ½ā£ŗ1-±ū“¼ÕōĘųÓėæÕĘų»ģŗĻĶعżČČĶĶų£¬Éś³ÉµÄ»ÆŗĻĪļĪŖCH3CH2CHO£¬
A£®CH3CH2CHOĪŖ±ūČ©£¬ĪŖĶ¬Ņ»ÖÖĪļÖŹ£¬²»ŹōÓŚĶ¬·ÖŅģ¹¹Ģ壬¹ŹB“ķĪó£»
B£®CH3CH2COOHÓėCH3CH2CHOµÄ·Ö×ÓŹ½²»ĻąĶ¬£¬²»ŹōÓŚĶ¬·ÖŅģ¹¹Ģ壬¹ŹB“ķĪó£»
C£®CH3COCH3ĪŖ±ūĶŖ£¬±ūĶŖCH3CH2CHOµÄ·Ö×ÓŹ½ĻąĶ¬£¬¶žÕߏōÓŚĶ¬·ÖŅģ¹¹Ģ壬¹ŹCÕżČ·£»
D£®CH3CH2OCH3ÓėCH3CH2CHO·Ö×ÓŹ½²»ĻąĶ¬£¬²»ŹōÓŚĶ¬·ÖŅģ¹¹Ģ壬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“·½·Ø£¬ĢāÄæÄŃ¶Č²»“ó£¬×¢ŅāÕĘĪÕĶ¬·ÖŅģ¹¹ĢåµÄøÅÄī¼°ŹéŠ“·½·Ø£¬ÕżČ·ÅŠ¶Ļ×ö1-±ū“¼øśŃõĘų·“Ó¦µÄ²śĪļŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬ŹŌĢāÅąŃųĮĖѧɜµÄĮé»īÓ¦ÓĆÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¼ĘĖćĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ŃōĄė×Ó | K+”¢Na+”¢NH4+”¢Fe2+”¢Ba2+”¢Cu2+ |
| ŅõĄė×Ó | OH-”¢I-”¢NO3-”¢AlO2-”¢HCO3-”¢HSO4- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3ÖÖ | B£® | 4ÖÖ | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā

 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A | B | C | D | |
| ·½°ø | 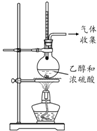 |  | 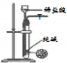 | 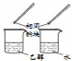 |
| ÄæµÄ | ĄūÓĆŅŅ“¼µÄĻūČ„·“Ó¦ÖĘČ”ŅŅĻ© | Õō·¢NH4Cl±„ŗĶČÜŅŗÖʱøNH4Cl¾§Ģå | ÖĘȔɣĮæ“æ¾»µÄCO2ĘųĢå | ±Č½ĻŅŅ“¼ÖŠōĒ»łĒāŌ×ÓŗĶĖ®·Ö×ÓÖŠĒāŌ×ӵĻīĘĆŠŌ |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| Ń”Ļī | ŹµŃé | ĻÖĻó | ½įĀŪ |
| A | ĻņKBrO3ČÜŅŗÖŠ¼ÓČėÉŁĮæ±½£¬Č»ŗóĶØČėÉŁĮæCl2 | ÓŠ»ś²ć³Ź³ČÉ« | Ńõ»ÆŠŌ£ŗCl2£¾KBrO3 |
| B | ĻņKNO3ŗĶKOH»ģŗĻČÜŅŗÖŠ¼ÓČėĀĮ·Ū²¢¼ÓČČ£¬½«ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½·ÅŌŚŹŌ¹ÜæŚ | ŹŌÖ½±äĪŖĄ¶É« | NO3-±»»¹ŌĪŖNH3 |
| C | Ļņ0.1mol•L-1µÄNa2CO3ČÜŅŗÖŠ¼ÓČėĮ½µĪ·ÓĢŖ£¬ČÜŅŗĻŌĒ³ŗģÉ«£¬Ī¢ČČ£® | ŗģÉ«¼ÓÉī | ŃĪĄąĖ®½āŹĒĪüČČ·“Ó¦ |
| D | ½«0.1mol•L-1µÄMgSO4ČÜŅŗµĪČėNaOHČÜŅŗÖĮ²»ŌŁÓŠ³Įµķ²śÉś£¬ŌŁµĪ¼Ó0.1mol•L-1µÄCuSO4ČÜŅŗ | °×É«³ĮµķÖš½„±äĪŖĄ¶É«³Įµķ | Ksp[Cu£ØOH£©2]£¼Ksp[Mg£ØOH£©2] |
| A£® | A | B£® | B | C£® | C | D£® | D |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
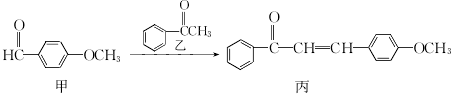
| A£® | ¼×ŗĶ±ū¾łÄÜŹ¹ĖįŠŌøßĆĢĖį¼ŲĶŹÉ« | |
| B£® | ŗĖ“Ź²ÕńĒāĘ×æÉŅŌĒų·ÖŅŅŗĶ±ū | |
| C£® | ŅŅÓė×ćĮæH2¼Ó³ÉĖłµĆµÄ²śĪļ·Ö×ÓÖŠÓŠ2øöŹÖŠŌĢ¼Ō×Ó | |
| D£® | 1mol¼×ŌŚŅ»¶ØĢõ¼žĻĀ×ī¶ąÓė4 molĒāĘų·¢Éś¼Ó³É·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com