
| A. | 除去MgCl2溶液中的Fe3+,可向溶液中加入氨水调节pH | |
| B. | 除去污水中的金属离子Cu2+、Hg2+,可向溶液中加入FeS | |
| C. | 除去Cl2中混有的HCl,可以将气体通入饱和氯化钠溶液 | |
| D. | 除去CaCO3中的少量CaSO4,可以向其中加入足量饱和Na2CO3溶液后过滤 |
分析 A.加入氨水,除去铁离子,但引入新杂质铵根离子;
B.Cu2+、Hg2+加入FeS均发生沉淀的转化,生成更难溶的物质;
C.HCl极易溶于水,食盐水可抑制氯气的溶解;
D.向其中加入足量饱和Na2CO3溶液,Qc(CaCO3)>Ksp(CaCO3).
解答 解:A.除去MgCl2溶液中的Fe3+,可向溶液中加入MgO(或氢氧化镁等)调节pH,且不引入新杂质,故A错误;
B.Cu2+、Hg2+加入FeS均发生沉淀的转化,生成更难溶的物质CuS、HgS,能除去污水中的金属离子Cu2+、Hg2+,故B正确;
C.HCl极易溶于水,食盐水可抑制氯气的溶解,则将气体通入饱和氯化钠溶液可除杂,故C正确;
D.向其中加入足量饱和Na2CO3溶液,Qc(CaCO3)>Ksp(CaCO3),生成CaCO3,然后过滤,滤纸上的物质为CaCO3,故D正确;
故选A.
点评 本题考查物质的分离和提纯,为高考常见题型,侧重于学生的分析能力和实验能力的考查,题目难度不大,注意把握除杂的原则及反应原理的应用.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
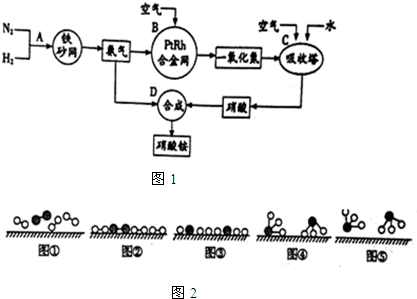
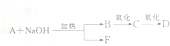
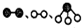 分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.
分别表示N2、H2、NH3.图⑤表示生成的NH3离开催化剂表面,图②和图③的含义分别是N2、H2被吸附在催化剂表面;在催化剂表面N2、H2中的化学键断裂.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +244.1 kJ•mol-1 | B. | -488.3 kJ•mol-1 | C. | -996.6 kJ•mol-1 | D. | +996.6 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
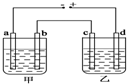 甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )
甲、乙两个相同的电解槽,如图所示连接a,b,c,d均为铂电极,通电后发现a极板处有气体放出,c极板质量增加,则以下说法中正确的是( )| A. | 甲槽中溶液是H2SO4,乙槽中溶液是NaOH | |
| B. | 甲槽中溶液是NaOH,乙槽中溶液是AgNO3 | |
| C. | 甲槽中溶液是AgNO3,乙槽中溶液是CuSO4 | |
| D. | 甲槽中溶液是CuSO4,乙槽中溶液是H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①②④ | C. | ②③ | D. | ④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酸性:H2SiO3>H2CO3>H3PO4 | B. | 稳定性:PH3<H2S<HCl<HF | ||
| C. | 非金属性:Cl>S>P>Si | D. | 离子半径:Cl->F->Na+>Al3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com