
| 实验次数编号 | 待测液体积mL | 滴入的标准液体积(mL) |
| 1 | 25.00 | 28.95 |
| 2 | 25.00 | 25.05 |
| 3 | 25.00 | 24.95 |
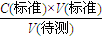 分析误差;
分析误差;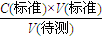 分析,可知C(标准)偏大,故①正确;
分析,可知C(标准)偏大,故①正确; 分析,可知C(标准)不变,故②正确;
分析,可知C(标准)不变,故②正确;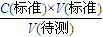 分析,可知C(标准)偏小,故③错误;
分析,可知C(标准)偏小,故③错误;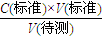 分析,可知C(标准)偏小,故④错误;
分析,可知C(标准)偏小,故④错误;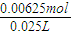 =0.25mol/L,故答案为:0.25.
=0.25mol/L,故答案为:0.25.

科目:高中化学 来源:江西省白鹭洲中学2012届高三上学期期中考试化学试题 题型:013
|
下列热化学方程式或离子方程式中,正确的是: | |
| [ ] | |
A. |
甲烷的标准燃烧热ΔH为-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3 kJ·mol-1 |
B. |
500℃、30 MPa下,将0.5 mol N2(g)和1.5 mol H2(g)置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为:N2(g)+3H2(g) |
C. |
向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO |
D. |
用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性: 2MnO |
查看答案和解析>>
科目:高中化学 来源:山东省青州一中2012届高三化学一轮跟踪训练:第11章 第4讲 醛 羧酸 酯(鲁科版) 题型:013
|
从甜橙的芳香油中可分离得到如下结构的化合物:
现有试剂: ①酸性KMnO4溶液; ②H2/Ni; ③Ag(NH3)2OH; ④新制Cu(OH)2悬浊液, 能与该化合物中所有官能团都发生反应的试剂有 | |
| [ ] | |
A. |
①② |
B. |
②③ |
C. |
③④ |
D. |
①④ |
查看答案和解析>>
科目:高中化学 来源:河北省正定中学2012届高三第二次综合考试化学试题 题型:013
|
下列热化学方程式或离子方程式中,正确的是 | |
| [ ] | |
A. |
甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为: CH4(g)+2O2(g)=CO2(g)+2H2O(g);ΔH=-890.3kJ·mol-1 |
B. |
500℃、30MPa下,将0.5 mol N2和1.5 mol H2置于密闭的容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: |
C. |
向明矾溶液中加入过量的氢氧化钡溶液:Al3++2SO42-+2Ba2++4OH-=2BaSO4↑AlO2-+2H2O |
D. |
用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
查看答案和解析>>
科目:高中化学 来源:江西省期中题 题型:单选题
 2NH3(g) △H= -38.6kJ/mol
2NH3(g) △H= -38.6kJ/mol 
查看答案和解析>>
科目:高中化学 来源: 题型:
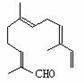
从甜橙的芳香油中可分离得到如右结构的化合物
现在试剂:①酸性KMnO4溶液;②H2/Ni;③Ag(NH3)2OH溶液;④新制Cu(OH)2悬浊液,能与该化合物中所有官能团都发生反应的试剂有
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com