
【题目】过渡元素Ti、Mn、Fe、Cu等可与C、H、O形成多种化合物。请回答下列问题:
(1)根据元素原子的外围电子排布的特征,可将元素周期表分成五个区域,其中Mn属于___区。
(2)Ti(BH4)2是一种过渡元素硼氢化物储氢材料。基态Ti2+中电子占据的最高能层符号为___,该能层具有的原子轨道数为___,BH4-的空间构型是___。
(3)在Cu的催化作用下,乙醇可被空气中氧气氧化为乙醛,乙醛分子中碳原子的杂化方式是___,乙醛分子中HCO的键角___乙醇分子中H-C-O的键角(填“大于”、“等于”或“小于”)。
(4)电镀厂排放的废水中常含有剧毒的CN-,可在TiO2的催化下,先用NaClO将CN-氧化成CNO-,再在酸性条件下CNO-继续被NaClO氧化成N2和CO2。
①H、C、N、O四种元素的电负性由小到大的顺序为___。
②与CN-互为等电子体微粒的化学式为___(写出一种即可)。
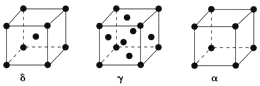
(5)单质铁有δ、γ、α三种同素异形体,三种晶胞中Fe原子的配位数之比为___,δ、γ、α三种晶胞的边长之比为___。
【答案】d M 9 正四面体型 sp3、sp2 大于 H<C<N<O CO(或N2等) 4:6:3 ![]() :
:![]() :1
:1
【解析】
(1)Mn为第ⅤⅢ族元素,最后填充电子为d电子;
(2)基态Ti2+价电子排布式为:3d2,最高能层为M层,该能层下含有1个3s轨道、3个3p轨道和5个3d轨道,共有9个原子轨道;BH4-中B原子价层电子对=4+![]() (3+1-4×1)=4,且没有孤电子对;
(3+1-4×1)=4,且没有孤电子对;
(3)乙醛分子中甲基上碳原子含有4个σ键,醛基上的碳原子含有3个σ键,据此判断碳原子的杂化方式,碳原子杂化方式不同导致其键角不同;
(4)①非金属性越强,电负性越大;
②等电子体中原子数、价电子数相同;
(5)δ-Fe为体心立方密堆积,配位数为8,γ-Fe为面心立方密堆积,配位数为12,α=Fe为简单立方堆积,配位数为6;设原子半径为y,δ中体对角线为4r,γ中面对角线为4r、α中棱长为2r,以此计算。
![]() 为第ⅤⅢ族元素,外围电子排布式为
为第ⅤⅢ族元素,外围电子排布式为![]() ,最后填充电子为d电子,则位于d区,故答案为:d;
,最后填充电子为d电子,则位于d区,故答案为:d;
![]() 的原子序数为22,
的原子序数为22,![]() 核外有20个电子,
核外有20个电子,![]() 的电子排布式为
的电子排布式为![]() 或
或![]() ,基态
,基态![]() 价电子排布式为:
价电子排布式为:![]() ,最高能层为M层,该能层下含有1个3s轨道、3个3p轨道和5个3d轨道,共有9个原子轨道,
,最高能层为M层,该能层下含有1个3s轨道、3个3p轨道和5个3d轨道,共有9个原子轨道,![]() 中B原子价层电子对
中B原子价层电子对![]() ,且没有孤电子对,则为正四面体型;
,且没有孤电子对,则为正四面体型;
![]() 乙醛分子中甲基上碳原子含有4个
乙醛分子中甲基上碳原子含有4个![]() 键,醛基上的碳原子含有3个
键,醛基上的碳原子含有3个![]() 键,所以甲基中的碳原子采用
键,所以甲基中的碳原子采用![]() 杂化,醛基中的碳原子采用
杂化,醛基中的碳原子采用![]() 杂化,醛基中碳原子采用
杂化,醛基中碳原子采用![]() 杂化、乙醇中含有醇羟基的碳原子采用
杂化、乙醇中含有醇羟基的碳原子采用![]() 杂化,导致乙醛分子中
杂化,导致乙醛分子中![]() 的键角大于乙醇分子中的
的键角大于乙醇分子中的![]() 的键角;
的键角;
![]() 非金属性越强,电负性越大,则电负性为
非金属性越强,电负性越大,则电负性为![]() ;
;
![]() 与
与![]() 互为等电子体微粒的化学式为
互为等电子体微粒的化学式为![]() 或
或![]() 等
等![]() ;
;
![]() 为体心立方密堆积,配位数为8,
为体心立方密堆积,配位数为8,![]() 为面心立方密堆积,配位数为12,
为面心立方密堆积,配位数为12,![]() 为简单立方堆积,配位数为6,则
为简单立方堆积,配位数为6,则![]() 、
、![]() 、
、![]() 三种晶胞中铁原子的配位数之比为8:12:
三种晶胞中铁原子的配位数之比为8:12:![]() :6:3,设Fe的原子半径为r,
:6:3,设Fe的原子半径为r,![]() 、
、![]() 、
、![]() 晶胞的边长分别为
晶胞的边长分别为![]() 、
、![]() 、
、![]() ,则
,则![]() 中
中![]() ,
,![]() 中
中![]() ,
,![]() 中
中![]() ,则边长之比为:
,则边长之比为:![]() :
:![]() :
:![]() :
:![]() :1。
:1。


 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源: 题型:
【题目】现有四种元素的基态原子的电子排布式如下:①![]() ;②
;②![]() ;③
;③![]() ;④
;④![]() 则下列有关比较中正确的是
则下列有关比较中正确的是![]()
A.第一电离能:③>②>④>①
B.原子半径:①>②>④>③
C.电负性:③>①>②>④
D.最高正化合价:③>①>②>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中发生反应N2+3H2![]() 2NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
2NH3,△H<0达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
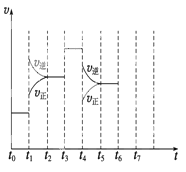
(1)处于平衡状态的时间段是 (填选项)。
A.t0~t1
B.t1~t2
C.t2~t3
D.t3~t4
E.t4~t5
F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是_____(填选项)。
A.增大压强
B.减小压强
C.升高温度
D.降低温度
E.加催化剂
F.充入氮气
t1时刻 ;t3时刻 ;t4时刻 。
(3)依据(2)中的结论,下列时间段中,氨的百分含量最高的是 (填选项)。
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6
(4)如果在t6时刻,从反应体系中分离出部分氨,t7时刻反应达到平衡状态,请在图中画出反应速率的变化曲线。
(5)一定条件下,合成氨反应达到平衡时,测得混合气体中氨气的体积分数为20%,则反应后与反应前的混合气体体积之比为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次硫酸钠甲醛(xNaHSO2yHCHOzH2O)俗称吊白块,在印染、医药以及原子能工业中有广泛应用。它的组成可通过下列实验测定:①准确称取1.5400g样品,完全溶于水配成100mL溶液。②取25.00mL所配溶液经AHMT分光光度法测得甲醛物质的量浓度为0.10mol×L-1。③另取25.00mL所配溶液,加入过量碘完全反应后,加入BaCl2溶液至沉淀完全,过滤、洗涤、干燥至恒重得到白色固体0.5825g。次硫酸氢钠和碘反应的方程式如下:xNaHSO2yHCHOzH2O+I2→NaHSO4+HI+HCHO+H2O(未配平)
(1)生成0.5825g白色固体时,需要消耗碘的质量为_____。
(2)若向吊白块溶液中加入氢氧化钠,甲醛会发生自身氧化还原反应,生成两种含氧有机物,写出该反应的离子方程式_____。
(3)通过计算确定次硫酸氢钠甲醛的组成______(写出计算过程)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示,电极为惰性电极。已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42—等离子。下列叙述中正确的是( )
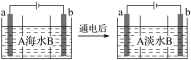
A. A膜是阳离子交换膜
B. 通电后,海水中阴离子往b电极处移动
C. 通电后,b电极上产生无色气体,溶液中出现白色沉淀
D. 通电后,a电极的电极反应式为4OH--4e-=O2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物在生活中处处可见,与人类关系密切,请回答:
(1)![]() 的分子式为_____________。
的分子式为_____________。
(2)写出![]() 中官能团的名称_________________。
中官能团的名称_________________。
(3)相对分子质量为72且沸点最低的烷烃的结构简式为__________________。
(4)相对分子质量为100的烷烃,其主链上有5个碳原子的同分异构体有_____种。
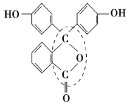
(5)酚酞是常用的酸碱指示剂,其结构简式如下所示:从结构上看酚酞可看作_________。
A.烯烃 B.芳香族化合物 C.醇类物质
D.酚类物质 E.醚类物质 F.酯类物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大气中CO2含量的增加会加剧温室效应,为减少其排放,需将工业生产中产生的CO2分离出来进行储存和利用。
(1)CO2与NH3反应可合成化肥尿素[化学式为CO(NH2)2],反应2NH3(g)+CO2(g)![]() CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[
CO(NH2)2(l)+H2O(g)在合成塔中进行。如图1中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比[![]() ]和水碳比[
]和水碳比[![]() ]投料时二氧化碳转化率的情况。
]投料时二氧化碳转化率的情况。
①曲线Ⅰ、Ⅱ、Ⅲ水碳比的数值范围分别为0.6~0.7、1~1.1和1.5~1.61,则生产中应选用水碳比的数值范围为_________________。
②请推测生产中氨碳比控制在4.0左右还是控制在4.5左右比较适宜,并简述你的理由__________________。
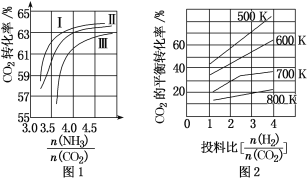
(2)CO2与H2也可用于合成甲醇:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
CH3OH(g)+H2O(g)。在体积可变的恒压密闭容器中,该反应在不同温度、不同投料比时,CO2的平衡转化率如图2所示。
①该反应的化学平衡常数的表达式为_______________________。
②该反应的ΔS___0
③已知: ① CO(g)+2H2(g) CH3OH(g) ΔH= -90.1 kJ·mol-1 ②CO(g) +H2O(g) CO2(g)+H2(g) ΔH= -41.1 kJ·mol-1,则CO2与H2反应合成CH3OH(g)的热化学方程式为___________________。
④700K投料比[![]() ]=2时,H2的平衡转化率为______________。
]=2时,H2的平衡转化率为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(g),2min末反应达到平衡状态, 生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
xC(g)+2D(g),2min末反应达到平衡状态, 生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于_____________
(2)A的转化率为_______________
(3)生成D的反应速率为_____________
(4)如果增大反应体系的压强,则平衡体系中C的质量分数 _________(填增大、减小或不变)
(5)在此温度下,该化学反应的平衡常数k=__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛镍形状记忆合金(TiNi)被广泛用于人造卫星和宇宙飞船的天线,在临床医疗领域内也具有广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式:_________,Ni在元素周期表中的位置是_________。
(2)钛镍合金能溶于热的硫酸生成Ti(SO4)2、NiSO4,二者阴离子的立体构型为______,中心原子的轨道杂化类型是_______。
(3)与钛同周期的另一种元素钴(Co)可形成分子式均为Co(NH3)5BrSO4的两种配合物,其中一种化学式为[Co(NH3)5Br]SO4,往其溶液中加BaCl2溶液时,现象是____________;往另一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则第二种配合物的化学式为 _______________ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com