
| A. | 按系统命名法,化合物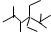 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 的名称是2,3,5,5-四甲基-4,4-二乙基己烷 | |
| B. | 可用热的饱和Na2CO3溶液除去金属表面的机油、润滑油 | |
| C. | C4H10的一氯取代物有4种 | |
| D. | 用酸性KMnO4溶液可鉴别2-丁烯和正丁醛 |
分析 A.该命名中,取代基的编号之和不是最小;
B.矿物油的成分是烃类,不与NaOH反应;
C.丁烷有2种同分异构体,然后根据氢原子的种类确定一氯代物的数目;
D.2-丁烯和正丁醛都能够被酸性高锰酸钾溶液氧化.
解答 解:A. 的命名中,编号应该从右边开始,在2号C含有2个甲基,在3号C含有2个乙基,则4、5号C各含有1个甲基,其正确命名为:2,2,4,5-四甲基-2,2-二乙基己烷,故A错误;
的命名中,编号应该从右边开始,在2号C含有2个甲基,在3号C含有2个乙基,则4、5号C各含有1个甲基,其正确命名为:2,2,4,5-四甲基-2,2-二乙基己烷,故A错误;
B.碳酸钠在溶液中发生水解溶液显碱性,加热使碳酸钠溶液碱性增强,能使动物或植物的油脂发生水解,但矿物油的成分是烃类,不与NaOH反应,故热的碳酸钠溶液不能去除金属表面的矿物油,故B错误;
C.丁烷(C4H10)有2种同分异构体:正丁烷和异丁烷,正丁烷有2种氢原子,异丁烷有2种氢原子,则C4H10的一氯取代物有4种,故C正确;
D.2-丁烯中的碳碳双键和正丁醛中的醛基都能够被酸性高锰酸钾溶液氧化,所以不能用酸性高锰酸钾溶液鉴别2-丁烯和正丁醛,故D错误;
故选C.
点评 本题考查较为综合,涉及有机物命名、有机物除杂与鉴别、同分异构体书写等知识,题目难度中等,明确常见有机物组成、结构与性质为解答关键,试题培养了学生的分析能力及灵活应用能力.


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
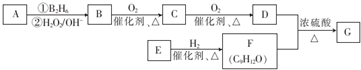
 ;该反应的反应类型为酯化反应或取代反应.
;该反应的反应类型为酯化反应或取代反应.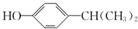 .
.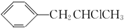 为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):
为原料也可合成F,请参考题目中的相关信息写出相应的合成路线图(反应条件中的试剂写在箭头上方,其他写在箭头下方):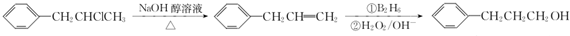 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO和HCl | B. | CH4和NH3 | C. | CH4和HCl | D. | H2和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
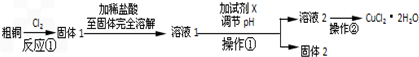
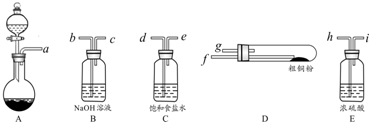
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
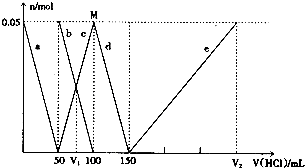
| A. | V1:V2=l:5 | |
| B. | M点时生成的CO2为0.05mol | |
| C. | 原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 | |
| D. | a曲线表示的离子方程式为:AlO2-+H++H2O═Al(OH)3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
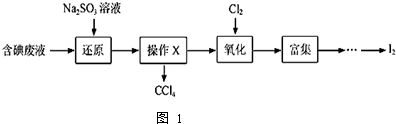
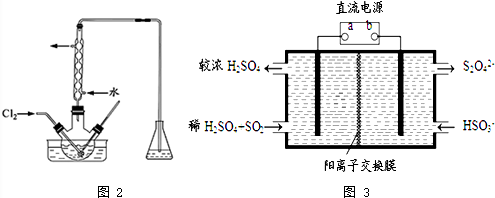
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3517Cl、3717Cl为不同核素,其化学性质不同 | |
| B. | 元素的相对原子质量,是按照该元素各种核素原子所占的一定百分比算出的平均值 | |
| C. | 目前已发现的所有元素占据了周期表里全部位置,不可能再有新的元素发现 | |
| D. | 常温常压下,非金属元素的原子都能形成气态单质分子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com